
| A. | 56g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA | |
| B. | 1mol 固体Na2O2含有的阴阳离子总数为3NA | |
| C. | 等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1 | |
| D. | 1L 1 mol•L-1的NaClO 溶液中含有ClO-的数目为NA |
分析 A、56g铁饭即1mol铁粉在1mol氯气中燃烧,铁粉过量;
B、过氧化钠由2个钠离子和1个过氧根构成;
C、磷酸为中强酸,不能完全电离;
D、次氯酸根为弱酸根,在溶液中会水解.
解答 解:A、56g铁饭即1mol铁粉在1mol氯气中燃烧,铁粉过量,氯气完全反应,而由于氯气反应后变为-1价,故1mol氯气得2mol电子,则铁粉失去的电子为2mol,即为2NA个,故A错误;
B、过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含3mol离子即3NA个,故B正确;
C、磷酸为中强酸,不能完全电离,故两溶液中电离出的氢离子的个数之比小于3:1,故C错误;
D、次氯酸根为弱酸根,在溶液中会水解,故溶液中的次氯酸根的个数小于NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③④⑤ | C. | ①③⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当它可以形成①时,不可能形成③ | B. | 当它形成①时,也可以形成②和③ | ||
| C. | 当它可以形成②时,不可能形成③ | D. | 当它可以形成①时,不可能形成② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于浓度差产生放热 | B. | 发生了水分解反应 | ||
| C. | 发生了盐分解反应 | D. | 盐的溶解程度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
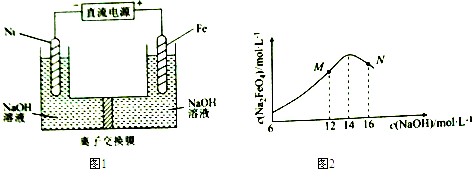
| A. | 制备Na2FeO4的电极反应为Fe-6e-+8OH-=FeO42-+4H2O | |
| B. | 电解过程中,须将阴极产生的气体及时排出 | |
| C. | MN两点中c(Na2FeO4)低于最高值的原因不同,在M点会有Fe(OH)3生成 | |
| D. | 图1中的离子交换膜为阴离子交换膜,电解过程中,阴极区附近pH会增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
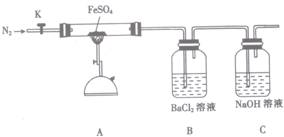
| 操作步骤 | 实验现象 | 用化学方程式解释原因 |
| 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | 洗气瓶B中①有白色沉淀生成 | ②SO3+H2O+BaCl2=BaSO4↓+2HCl |
| A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到③有红棕色固体物质生成 | ④2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑ |
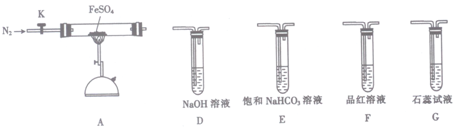
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)<c(OH-)<c(B+)<c(A-) | B. | c(H+)<c(OH-)<c(A-)<c(B+) | ||
| C. | c(OH-)<c(H+)<c(B+)<c(A-) | D. | c(A-)=c(B+)>c(H+)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com