
X��Y��Z��W��R��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ��������Ϣ���±���
| Ԫ�� | �����Ϣ |
| X | ��ɵ����ʵĻ���Ԫ�أ�����������ϼ���������ϼ۵Ĵ�����Ϊ2 |
| Y | �ؿ��к�����ߵ�Ԫ�� |
| Z | ����������Ϊ23��������Ϊ11�ĺ��� |
| W | �����д���ʹ����Ͻ���Ʒ����ҵ�Ͽ��õ������������ķ����Ʊ��䵥�� |
| R | �ж��ֻ��ϼۣ����ɫ���������ڿ����л�Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ |
(1) W��Ԫ�����ڱ��е�λ��Ϊ �� X��Z��W����Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳���� (��Ԫ�ط��ű�ʾ)��
(2) X������Ԫ�ذ�ԭ����Ŀ��1��3��2��4���ɷ���A��B��A�ĵ���ʽΪ ��B�ĽṹʽΪ ��������ZY�д��ڵĻ�ѧ������Ϊ ��
(3) ��(As)������������Ԫ�أ���Xͬһ���壬Asԭ�ӱ�Xԭ�Ӷ��������Ӳ㣬�����ԭ������Ϊ �������������Ļ�ѧʽΪ ������2~4����Ԫ�ص���̬�⻯����ȶ��ԴӴ�С��˳���� (�û�ѧʽ��ʾ)��
(4) ��RCl3��Һ��ʴͭ��·������ӷ���ʽΪ ��������Һ��R3+���õ��Լ��� �����Թ۲쵽�������� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ����
A��������������Һ���ն���������2OH����2NO2===NO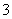 ��NO����H2O
��NO����H2O
B��̼��������Һ���������ʯ��ˮ��2HCO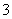 ��Ca2����2OH��===CaCO3����CO
��Ca2����2OH��===CaCO3����CO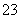 ��2H2O
��2H2O
C��Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��
2MnO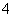 ��6H����5H2O2===2Mn2����5O2����8H2O
��6H����5H2O2===2Mn2����5O2����8H2O
D������������Һ���������������Һ��ϣ�H����SO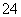 ��Ba2����OH��===BaSO4����H2O
��Ba2����OH��===BaSO4����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���У���ȷ���� ( )
A����״���£�1mol�κ����ʵ������ԼΪ22.4L
B��1mol�κ�������������������ͬ�����Ҳ��ԼΪ22.4L
C�����³�ѹ�£�����Mg���������û���1molH2ʱʧȥ�ĵ�����ԼΪ 1.204��1024
D��ͬ��ͬѹ�£���ͬ������κ����嵥������ԭ����Ŀ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ��
A�����������Һ�м�������������Һ��Ba2����SO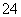 ===BaSO4��
===BaSO4��
B��˫��ˮ�м���ϡ�����KI��Һ��H2O2��2H����2I��===I2��2H2O
C����CH3COOH�ܽ�CaCO3��CaCO3��2H��=Ca2����H2O��CO2��
D��Na2S2O3��Һ�м���ϡ���2S2O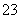 ��4H��===SO
��4H��===SO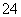 ��3S����2H2O
��3S����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
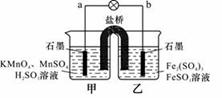
ij����ѧϰС���ͬѧ��������������ԭ��Ӧ���ԭ��أ�
2KMnO4��10FeSO4��8H2SO4==2MnSO4��5Fe2(SO4)3��K2SO4��8H2O ������װ�б���K2SO4��Һ��
������������ȷ����
A�����ձ��з�����ԭ��Ӧ
B�����ձ�����Һ��pH��С
C����ع���ʱ�������е�SO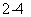 ������ձ�
������ձ�
D�����·�ĵ��������Ǵ�a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ס������������ڶ�����A��B�ķ�Ӧ����������ÿ���Ӽ�����4mol A����������ÿ���Ӽ���2mol A����������ڵķ�Ӧ���ʱ��������ڵķ�Ӧ���ʣ�������
| �� | A�� | �� | B�� | �� | C�� | ��� | D�� | ���ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�Ȼ�ѧ����ʽ��
H2O(g)��H2(g) +  O2(g) ��H = +241.8kJ��mol
O2(g) ��H = +241.8kJ��mol
H2(g)+  O2(g) �� H2O(1) ��H = ��285.8kJ��mol
O2(g) �� H2O(1) ��H = ��285.8kJ��mol
��1gҺ̬ˮ��Ϊˮ����ʱ���������仯��
A������88kJ B�� ����2.44KJ C������44kJ D�� ����44KJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴Ӧa A��s����b B��g�� c C��g����d D��g������Ӧ�����У���������������ʱ��C�İٷֺ�����C�������¶ȣ�T����ѹǿ��P���Ĺ�ϵ����ͼ����������ȷ���ǣ� ��
c C��g����d D��g������Ӧ�����У���������������ʱ��C�İٷֺ�����C�������¶ȣ�T����ѹǿ��P���Ĺ�ϵ����ͼ����������ȷ���ǣ� ��
A����ƽ����������C������
B����ƽ��������£�ƽ������
C����ѧ����ʽ��b ��c +d
D����ƽ�������A����������ƽ�������ƶ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�йغϽ��������ȷ����(����)
A���Ͻ�ĵ����Աȳɷֽ���ǿ
B���Ͻ�Ŀ���ʴ���ܶ��ܺ�
C���Ͻ�Ļ�еǿ�ȱȸ��ɷֽ���С
D�������Ͻ�ȳɷֽ����۵�ͣ�Ӳ�ȴ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com