
已知铅的化合价有+2;+4,若将磁铁矿 看成“混合氧化物”可以写成
看成“混合氧化物”可以写成 ,若将其看成盐则可以写成
,若将其看成盐则可以写成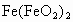 .已知高价态的金属氢氧化物一般酸性较强,根据以上信息和化合价规则,
.已知高价态的金属氢氧化物一般酸性较强,根据以上信息和化合价规则, 可以分别写成________和________.等物质的量的 和 分别和浓盐酸反应时,所消耗HCl的物质的量相等,不同的是,高价的铅能将盐酸氧化而放出氯气.试写出
可以分别写成________和________.等物质的量的 和 分别和浓盐酸反应时,所消耗HCl的物质的量相等,不同的是,高价的铅能将盐酸氧化而放出氯气.试写出 ,
, .分别和浓盐酸反应的化学方程式:_____________________、________________________.
.分别和浓盐酸反应的化学方程式:_____________________、________________________.
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:阅读理解



| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
已知铅的化合价有+2;+4,若将磁铁矿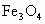 看成“混合氧化物”可以写成
看成“混合氧化物”可以写成 ,若将其看成盐则可以写成
,若将其看成盐则可以写成 .已知高价态的金属氢氧化物一般酸性较强,根据以上信息和化合价规则,
.已知高价态的金属氢氧化物一般酸性较强,根据以上信息和化合价规则,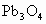 可以分别写成________和________.等物质的量的 和 分别和浓盐酸反应时,所消耗HCl的物质的量相等,不同的是,高价的铅能将盐酸氧化而放出氯气.试写出
可以分别写成________和________.等物质的量的 和 分别和浓盐酸反应时,所消耗HCl的物质的量相等,不同的是,高价的铅能将盐酸氧化而放出氯气.试写出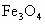 ,
,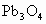 .分别和浓盐酸反应的化学方程式:_____________________、________________________.
.分别和浓盐酸反应的化学方程式:_____________________、________________________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省六市高三第二次联考化学试卷(解析版) 题型:填空题
高锰酸钾和二氧化锰是中学化学常用的化学试剂。根据下面相关的信息回答下列问题:
(1)已知: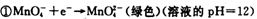
②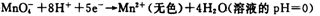
锰有多种化合价,如+7、十6、+4、+2价等,在中性溶液里高锰酸钾的还原产物为 (填化学式)。
(2)查阅相关资料:发生如下反应(反应未配平):

已知在高锰酸钾固体表面滴加浓盐酸,发生的半反应为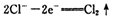
如果在盛有氯化锰溶液的试管中加入适量XeO3,振荡试管,可能观察到的现象是 。
(3)已知草酸(H2C2O4)为二元弱酸,取少量草酸晶体溶于酸性高锰酸钾溶液,溶液的紫色褪去。
写出该反应的离子方程式 。
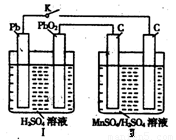
(4)MnO2是一种重要的无机功能材料,制备MnO2的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为 。现以铅蓄电池为电源电解酸化的MnSO4溶液,如图所示,铅蓄电池的总反应方程式为 ,当蓄电池中有4mol H+被消耗时,则电路中通过的电子的物质的量为 ,MnO2的理论产量为 g。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省资阳市高三第二次高考模拟考试理综化学试卷(解析版) 题型:推断题
A、B、C、D、E、F为前四周期的元素。其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为紫红色固体,可通过“湿法冶金”而得。请回答下列问题:
(1)CB3分子中心原子的杂化类型是 。
(2)F元素的原子的外围电子排布式为 ;如图所示为F与Au以3∶1形成的合金晶胞图,在图中的括号内写出对应的元素符号。

(3)B、D元素最高价氧化物对应的水化物的酸性强弱: > (填化学式)。
(4)用导线将A和F的单质做成的电极连接起来,插入到盛有C的最高价氧化物的水化物的浓溶液中构成原电池,试写出在单质A表面发生反应的电极反应式:_____。
(5)分子R是由C元素与氢元素形成的18电子分子,R的电子式为 。
(6)24 g E的单质在33.6 L氧气(标准状况)中燃烧,至反应物全部耗尽,放出x kJ热量。则1mol E与O2反应生成E的低价氧化物时的热化学方程式为 (已知:E的燃烧热为y kJ/mol)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com