
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O (g)△H=-890.3 kJ•mol-1 | |
| B. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g) 不能自发进行,则该反应的△H<0 | |
| D. | 已知①2H2(g)+O2(g)═2H2O (g)△H1=a kJ•mol-1②2H2(g)+O2(g)═2H2O (l)△H2=b kJ•mol-1,则a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
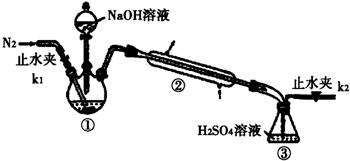
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 化合物AE与CE含有不同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 168O、178O、188O属于同位素 | |
| B. | N60和N2互为同系物 | |
| C. | O2和O3、H2和D2、H218O和H216O都互为同素异形体 | |
| D. | CH2O2、C2H4O2、C3H6O2、C4H8O2互为同系物;乙二醇、丙三醇也互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
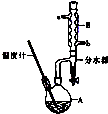 B正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:
B正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:| 相对分子质量 | 沸点/℃ | 密度(g/cm3) | 水中溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.819 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com