
��һ�������£�N2O�ֽ�IJ���ʵ���������£�
| ��Ӧʱ ��/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| c(N2O)/ (mol·L��1) | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
��ͼ����ȷ��ʾ�÷�Ӧ�й��������仯���ɵ���(����)
(ע��ͼ�а�˥��ָ��һŨ��N2O����һ��ʱ�������Ӧʱ�䣬c1��c2����ʾN2O��ʼŨ����c1<c2)
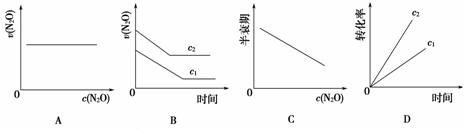
�������ɱ����е����ݿ�֪��ÿ��ʱ�����N2O������ȣ�A��ȷ��B����C��ɱ������ݿ�֪��c(N2O)��0.100��0.050����50 min��c(N2O)��0.080��0.040����40 min��c(N2O)��0.060��0.030����30 min��c(N2O)��0.020��0.010����10 min����c(N2O)Խ��˥��Խ����D��ɱ������ݿ�֪��Ũ��Խ����ͬʱ����N2O��ת����ԽС������c1<c2��Ũ��Ϊc1ʱ��ת���ʴ���Ũ��Ϊc2ʱ��ת���ʣ�����
�𰸡�A


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���д�ʩ������Ӧ����������Ч����( )
A.Al��������ȼ������Al2O3������Ƭ�ij�����
B.Fe��ϡ���ᷴӦ��ȡH2ʱ������Ũ����
C.��K2SO4��BaCl2����Һ��Ӧʱ������ѹǿ
D.Na��ˮ��Ӧʱ����ˮ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ԫ�����ڱ������ڵ�һ������ͼ��ʾ�������й�A��B��C��D��E����Ԫ�ص������У���ȷ����(����)
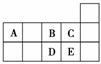
A��D�ڹ�����B��ȼ�յ���Ҫ����ΪDB3
B��C���⻯���ˮ��Һ���Ա�E��ǿ
C��A��B�γɵ������ӿ�����AB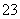 ��A2B
��A2B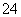
D��E�����������γ�����������Ժ�����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��25�桢101 kPa�����£�C(s)��H2(g)��CH3COOH(l)��ȼ���ȷֱ�Ϊ393.5 kJ·mol��1��285.8 kJ·mol��1��870.3 kJ·mol��1����2C(s)��2H2(g)��O2(g)===CH3COOH(l)�ķ�Ӧ��Ϊ(����)
A����488.3 kJ·mol��1 B����488.3 kJ·mol��1
C����191 kJ·mol��1 D����191 kJ·mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��CaSO4����O2��ȼ��CO��Ӧ���ȿ����ȼ��Ч�ʣ����ܵõ��ߴ�CO2����һ�ָ�Ч����ࡢ���õ�����ȼ�ռ�������Ӧ��Ϊ����Ӧ����Ӧ�ں͢�Ϊ����Ӧ��
�� 1/4CaSO4(s)��CO(g)1/4CaS(s)��CO2(g)
��H1����47.3 kJ·mol��1
�� CaSO4(s)��CO(g)CaO(s)��CO2(g) ��SO2(g)
��H2����210.5 kJ·mol��1
�� CO(g)1/2C(s)��1/2CO2(g)����H3����86.2 kJ·mol��1
��Ӧ2CaSO4(s)��7CO(g)CaS(s)��CaO(s)��6CO2(g)��C(s)��SO2(g)�Ħ�H��________(�æ�H1����H2�ͦ�H3��ʾ)
(2)[2014·ȫ���¿α��28(2)]��֪��
�״���ˮ��Ӧ
2CH3OH(g)===CH3OCH3(g)��H2O(g)����H1����23.9 kJ·mol��1
�״���ϩ����Ӧ
2CH3OH(g)===C2H4(g)��2H2O(g)����H2����29.1 kJ·mol��1
�Ҵ��칹����Ӧ
C2H5OH(g)===CH3OCH3(g)����H3����50.7 kJ·mol��1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4(g)��H2O(g)===C2H5OH(g)�Ħ�H��________kJ·mol��1��
(3)[2014·�Ĵ����ۣ�11(3)]��֪��25 �桢101 kPaʱ��
Mn(s)��O2(g)===MnO2(s)����H����520 kJ·mol��1
S(s)��O2(g)===SO2(g)����H����297 kJ·mol��1
Mn(s)��S(s)��2O2(g)===MnSO4(s)����H����1 065 kJ·mol��1
SO2��MnO2��Ӧ������ˮMnSO4���Ȼ�ѧ����ʽ��__________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���¶�����ij�ݻ��̶����ܱ������м���2 mol A��1 mol B���������·�Ӧ��2A(g)��B(g)3C(g)��D(s)����H����Q kJ·mol��1(Q��0)
����Ӧ�ﵽƽ���Ӧ�ų�������ΪQ1 kJ������A��ת����Ϊ������ش��������⣺
(1)Q1________Q(�����������������)������__________________________________________________________
__________________________________________________________��
(2)A��ת���ʦ���________(�ú�Q��Q1�Ĵ���ʽ��ʾ)��ƽ�����������������D��A��ת����________(���������С�����䡱)��
(3)��Ӧ�ﵽƽ����������¶ȣ�K________(���������С�����䡱)����������ƽ����Է�������________(���������С�����䡱)��
(4)ά���¶Ⱥ������������䣬����ʼʱ�������м���������������ĸ�ѡ���Ӧ�ﵽƽ���ų���������ΪQ1 kJ����(ϡ�����岻���뷴Ӧ)________(�����)��
A��2 mol A��1 mol B��1 mol Ar
B��3 mol C��1 mol D
C��1 mol A��0.5 mol B��1.5 mol C��0.5 mol D
D��2 mol A��1 mol B��1 mol D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б仯���������仯���ǣ�������
| �� | A�� | �����ڷŵ������±�ɳ��� |
| �� | B�� | ���ȵ����ɰ�ɫ��ˮ����ͭ |
| �� | C�� | Ư�IJ�ñ�����ڿ����б�� |
| �� | D�� | ����̿ʹ��īˮ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�����Һ���������Ӽ���Ũ�������ʾ��������Һ�е�OH﹣������M����Ϊ��������
| ���� | NO3﹣ | SO42﹣ | H+ | M |
| Ũ��/mol•L﹣1 | 2 | 1 | 2 | 1 |
| �� | A�� | Cl﹣ | B�� | Ba2+ | C�� | NO3﹣ | D�� | Mg2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʽΪC4H9Cl��ͬ���칹���У�������
| �� | A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com