


科目:高中化学 来源: 题型:
| 实验步骤 | 预期现象和结论 |
| 步骤1:用试管取样品溶液2~3mL,再用滴管取 | 若出现血红色,则假设1成立; 若未出现血红色,则假设2或假设3成立. |
| 步骤2: | 结合步骤1的现象和结论, |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )| A、原合金质量为0.92g |
| B、标准状况下产生氢气896mL |
| C、图中V2为60mL |
| D、图中m值为1.56g |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:mA(s)+nB(g)?pC(g)+q(D)g.达到平衡后,测得B的浓度为0.5mol/L.保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.2mol/L.当其条件不变时,C在反应混合物中的体积分数(x)与温度(T)、时间(t)的关系如图所示,下列叙述正确的是( )
一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:mA(s)+nB(g)?pC(g)+q(D)g.达到平衡后,测得B的浓度为0.5mol/L.保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.2mol/L.当其条件不变时,C在反应混合物中的体积分数(x)与温度(T)、时间(t)的关系如图所示,下列叙述正确的是( )| A、容积扩大到原来的两倍,平衡向逆反应方向移动 |
| B、化学方程式中n>p+q |
| C、达到平衡后,若升高温度,平衡向逆反应方向移动 |
| D、达到平衡后,增加A的量,有利于提高B的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
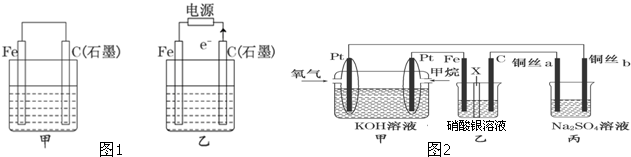
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口附近 |
| B、蒸发操作时,应使混合物的水分完全蒸干后才能停止加热 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,应选择有机萃取剂,它与原溶剂应互不相溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应物X与中间体Y互为同分异构体 |
| B、用一个氯原子取代X苯环上氢,产物只有3种 |
| C、普罗帕酮分子中有2个手性碳原子 |
| D、X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 原子序数依次增大的X、Y、Z、M、N五种元素,XZ2是引起温室效应的主要气体,M
原子序数依次增大的X、Y、Z、M、N五种元素,XZ2是引起温室效应的主要气体,M查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150ml 1 mol?L-1氯化钠溶液 |
| B、75ml 2 mol?L-1氯化镁溶液 |
| C、50ml 3mol?L-1氯化钾溶液 |
| D、200ml 1.5 mol?L-1氯化铁溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com