
| A. | 溴苯中含有溴单质,可用NaOH溶液洗涤,再经分液而除去 | |
| B. | 硝基苯中混有的硫酸和硝酸可用NaOH溶液洗涤,再经分液而除去 | |
| C. | 苯中的少量苯酚可用NaOH溶液洗涤,再经分液而除去 | |
| D. | 苯中的少量苯酚可加入浓溴水,再经过滤而除去 |
分析 A.溴能和NaOH反应生成可溶性的钠盐,溴苯和NaOH溶液不反应,且混合时分层;
B.硫酸、硝酸都能和NaOH溶液反应生成可溶性的钠盐,硝基苯和NaOH不反应,且和NaOH溶液不互溶;
C.苯酚和NaOH反应生成可溶性的苯酚钠,苯和NaOH不反应且混合时分层;
D.苯、苯酚和三溴苯酚都互溶.
解答 解:A.溴能和NaOH反应生成可溶性的钠盐,溴苯和NaOH溶液不反应,且混合时分层,然后用分液方法分离提纯,所以可以用NaOH溶液除去溴苯中的溴,故A正确;
B.硫酸、硝酸都能和NaOH溶液反应生成可溶性的钠盐,硝基苯和NaOH不反应,且和NaOH溶液不互溶,然后用分液方法分离提纯,所以可以用NaOH溶液除去硝基苯中的硫酸、硝酸,故B正确;
C.苯酚和NaOH反应生成可溶性的苯酚钠,苯和NaOH不反应且混合时分层,然后用分液方法分离提纯,所以可以用NaOH溶液除去苯中的苯酚,故C正确;
D.苯、苯酚和三溴苯酚都互溶,所以不能用浓溴水除去苯中的苯酚,应该用NaOH溶液,然后采用分液方法分离,故D错误;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及物质分离和提纯,明确物质性质差异性是解本题关键,侧重考查学生分析判断能力,注意:除杂时要除去杂质且不能引进新的杂质,除杂操作要简单易行.


科目:高中化学 来源: 题型:解答题
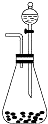 如图是一套实验室制气装置,某课外活动小组欲利用这套装置快速制取氧气和氯化氢气体,供选用的试剂有:A.浓H2SO4,B.浓盐酸,C.食盐,D.MnO2,?E.H2O2(aq)?,F.KClO3,G.KMnO4溶液,试完成下列问题:
如图是一套实验室制气装置,某课外活动小组欲利用这套装置快速制取氧气和氯化氢气体,供选用的试剂有:A.浓H2SO4,B.浓盐酸,C.食盐,D.MnO2,?E.H2O2(aq)?,F.KClO3,G.KMnO4溶液,试完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
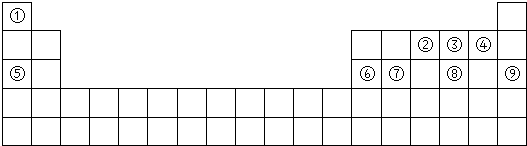
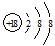
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
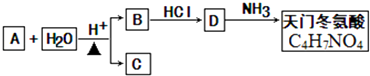
 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
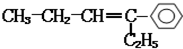 ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )| A. | 4,3,10 | B. | 4,3,12 | C. | 4,2,7 | D. | 4,5,10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 变为原来的10-3倍 | B. | 变为原来的10-2倍 | ||
| C. | 变为原来的10倍 | D. | 不发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
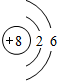 ,B的离子结构示意图
,B的离子结构示意图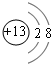 ,D的单质分子的电子式
,D的单质分子的电子式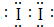 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com