


 ,反应类型为取代反应
,反应类型为取代反应 +n
+n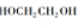 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$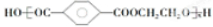 +(2n-1)H2O
+(2n-1)H2O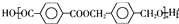 的路线流程图:
的路线流程图: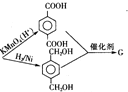 合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3. 分析 E的核磁共振氢谱为2组峰,且面积比为4:2,结合A的分子式可知,A的不饱和度为:$\frac{8×2+2-6}{2}$=6,E是D被酸性高锰酸钾氧化生成,且E能够C2H6O2反应生成高分子化合物F,则E分子中含有两个羧基,还应该含有苯环,且具有对称结构,故E的结构简式为: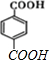 ;D的结构简式为:
;D的结构简式为: ;E生成F的反应为:n
;E生成F的反应为:n +n
+n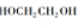 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$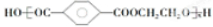 +(2n-1)H2O;C发生信息反应ii.生成D,则C的结构简式为:
+(2n-1)H2O;C发生信息反应ii.生成D,则C的结构简式为: ;A发生信息反应i.生成B,B与氯气发生取代反应生成C,则A为
;A发生信息反应i.生成B,B与氯气发生取代反应生成C,则A为 、B为
、B为 ,据此进行解答.
,据此进行解答.
解答 解:E的核磁共振氢谱为2组峰,且面积比为4:2,结合A的分子式可知,E的不饱和度为:$\frac{8×2+2-6}{2}$=6,E是D被酸性高锰酸钾氧化生成,且E能够C2H6O2反应生成高分子化合物F,则E分子中含有两个羧基,还应该含有苯环,且具有对称结构,故E的结构简式为: ;D的结构简式为:
;D的结构简式为: ;E生成F的反应为:n
;E生成F的反应为:n +n
+n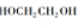 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$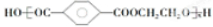 +(2n-1)H2O;C发生信息反应ii.生成D,则C的结构简式为:
+(2n-1)H2O;C发生信息反应ii.生成D,则C的结构简式为: ;A发生信息反应i.生成B、B与氯气发生取代反应生成C,则A为
;A发生信息反应i.生成B、B与氯气发生取代反应生成C,则A为 、B为
、B为 ,
,
(1)根据分析可知,A的结构简式为: ,
,
故答案为: ;
;
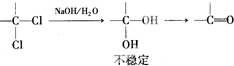
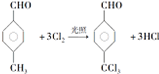
(2)B→C为 在光照条件下与氯气发生取代反生成
在光照条件下与氯气发生取代反生成 ,反应的化学反应方程式为:
,反应的化学反应方程式为: ,
,
故答案为: ;取代反应;
;取代反应;
(3)D的结构简式为: ,其名称为对醛基苯甲酸;E→F的化学反应方程式为:n
,其名称为对醛基苯甲酸;E→F的化学反应方程式为:n +n
+n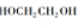 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$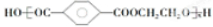 +(2n-1)H2O,
+(2n-1)H2O,
故答案为:对醛基苯甲酸;n +n
+n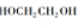 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$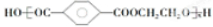 +(2n-1)H2O;
+(2n-1)H2O;
(4)B为 ,只有苯环,不存在其他环的B的同分异构体中,侧链可能含有醛基或碳碳双键或羰基,若为醛基时,可能的结构简式有:
,只有苯环,不存在其他环的B的同分异构体中,侧链可能含有醛基或碳碳双键或羰基,若为醛基时,可能的结构简式有: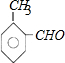 、
、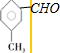 、
、 ,总共有3种;若为羰基,存在1种同分异构体;若含有碳碳双键,则取代基为:-CH=CH2和-OH,侧重邻、间、对3种结构,所以总共含有7种同分异构体,
,总共有3种;若为羰基,存在1种同分异构体;若含有碳碳双键,则取代基为:-CH=CH2和-OH,侧重邻、间、对3种结构,所以总共含有7种同分异构体,
故答案为:7;
(5)利用 、CH3Cl选择合适的无机试剂,补充完成合成G:
、CH3Cl选择合适的无机试剂,补充完成合成G: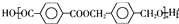 ,根据逆合成法,G水解会生成
,根据逆合成法,G水解会生成 和
和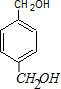 ,结合反应条件可知,
,结合反应条件可知, 和
和 需要通过
需要通过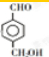 分别发生氧化和还原反应获得,结合题中反应信息用
分别发生氧化和还原反应获得,结合题中反应信息用 合成
合成 的流程为:
的流程为: ,
,
故答案为: .
.
点评 本题考查了有机合成,题目难度较大,根据题干流程明确合成原理为解答关键,注意掌握常见有机物结构与性质,明确同分异构体数目的求算方法,(5)为难点,需要结合题中反应原理利用逆合成法解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
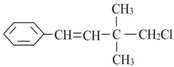 ,关于该有机物,下列叙述不正确的是( )
,关于该有机物,下列叙述不正确的是( )| A. | 所有碳原子不可能在同一平面上 | |
| B. | 属于卤代烃 | |
| C. | 分子式为C12H15Cl | |
| D. | 能发生加成反应、取代反应、加聚反应、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和甲醇 | B. | 邻羟基苯甲醛与对羟基苯甲醛 | ||
| C. | 对羟基苯甲酸与邻羟基苯甲酸 | D. | H2O和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
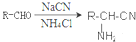 ,②
,②
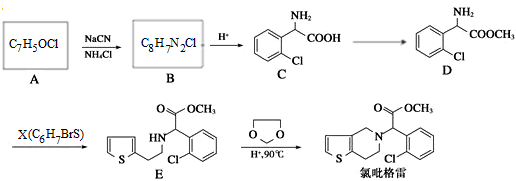
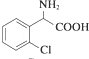 +CH3OH $→_{△}^{浓硫酸}$
+CH3OH $→_{△}^{浓硫酸}$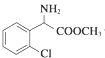 +H2O,反应类型取代反应.
+H2O,反应类型取代反应.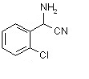 ,X
,X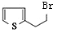 .
.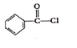 .
. .
.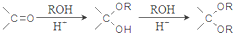 ,设计一条由乙烯、甲醇为有机原料制备化合物
,设计一条由乙烯、甲醇为有机原料制备化合物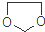 的合成路线流程图,无机试剂任选.(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)
的合成路线流程图,无机试剂任选.(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气在放电条件下变成臭氧 | B. | 加热胆矾成白色无水硫酸铜 | ||
| C. | 漂白的草帽久置空气中变黄 | D. | 氢氧化铁胶体加入硫酸镁产生沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com