
(1)请从下面的仪器中选择制取氨气的发生装置。(要求使用仪器最少、合理,写序号。)
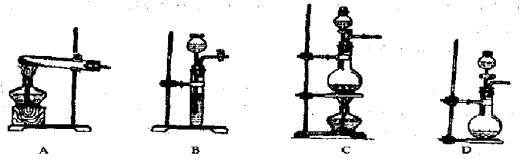
(2)写出用NH4Cl浓溶液与生石灰反应制取氨气的理由。
(3)实验操作时,关键之处是 ,理由是
(4)干燥氨气应选用的干燥剂是 。
| (1)D
(2)生石灰遇水生成氢氧化钙并放热,氢氧化钙和氯化铵受热生成氨气,或CaO+H2O=Ca(OH)2,放热反应,Ca(OH)2+2NH4Cl (3)将NH4Cl浓溶液逐滴滴加到生石灰中;生石灰充分吸收水,在水较少条件下反应易生成NH3气 (4)碱石灰或NaOH晶体
|
| 生石灰和水反应即生成氢氧化钙,氢氧化钠和氯化铵共热生成氨气。
A装置用于固体和固体物质在加热条件下的反应,此反应属于固体和液体试剂的反应,所以不能用A装置。B装置用于块状固体和液体不需要加热时的反应,且生成的气体不溶于或微溶于水,而生石灰遇水即成粉末状,且生成的氨气极易溶于水,故B装置也不符合要求。由于生石灰溶于水放出大量热,足以供给反应所需热量,此反应可不用酒精灯加热。所以D装置最简单。 由于生成的氨气极易溶于水,故应将NH4Cl浓溶液逐滴滴加到生石灰中,生石灰充分吸收水,在水较少条件下反应易生成NH3气逸出。 生成的氨气是碱性气体,应选择碱性干燥剂干燥。
|


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaCl晶体 C.NaOH溶液 D.CaO |
a.蒸馏 b.分液 c.盐析、过滤 d.萃取 |
① | ||
| ②乙醇(水) | ② | ||||
| ③肥皂(甘油、水) | ③ | ||||
| ④乙酸乙酯(乙酸) | ④ | ||||
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
化学在环境监测中越来越显示其重要作用,水体受还原性物质(主要是有机物)污染的程度常用化学需氧量(COD)来衡量。COD是指在一定条件下,用强氧化剂处理一定体积水样时所消耗的强氧化剂相当于氧气的质量,单位用mg/L表示。
重铬酸钾法是指在强酸性溶液中,用一定量的重铬酸钾氧化(以Ag+作催化剂)水样中的还原性物质,其本身被还原为Cr3+,过量的重铬酸钾以试亚铁灵作指示剂、用硫酸亚铁铵溶液回滴,根据相关试剂的用量即可求出水样的化学需氧量(COD)。
请回答下列问题:
(1)当水样中含有浓度较高的Cl-时,常需加入HgSO4溶液,则HgSO4的作用及可能原因是 。
(2)滴定时硫酸亚铁铵溶液需盛放在 (填“酸”或“碱”)式滴定管中。
(3)国家《生活饮用水标准检验法(GB5750-85)》中酚类的检测下限为0.002 mg/L。某水源受化工厂污染,酚含量达0.282 mg/L,该污染的水样中酚(以苯酚氧化成CO2计算)引起的化学需氧量(COD)为 mg/L。
(4)某化工园区有两家企业排放出的废水中,某次COD测量值高达2100 mg/L,这两家企业最有可能是 。(填字母)
a.制糖厂 b.水泥厂 c.电镀厂 d.造纸厂
(5)现有某废水样品10.00 mL,先加入10 mL蒸馏水,然后加入10.00 mL 0.04000 mol/L K2Cr2O7溶液、3 mL 1%硫酸-硫酸银溶液、17 mL硫酸汞溶液,加热反应2 h。在试亚铁灵指示剂存在下用0.1000 mol/L Fe(NH4)2(SO4)2溶液滴定多余的K2Cr2O7,共用去Fe(NH4)2(SO4)2溶液12.00 mL。试计算该水样的化学需氧量(COD)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com