
分析 水的电离是吸热过程,升高温度促进水电离,导致水的离子积常数增大;该温度下pH=1的硫酸中c(H+)=0.1mol/L、pH=11的NaOH溶液中c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$mol/L=0.01mol/L,要使混合溶液呈中性,说明n(H+)=n(OH-).
解答 解:水的电离是吸热过程,升高温度促进水电离,导致水的离子积常数增大,该温度下KW=1×10-13>1×10-14,说明该温度大于25℃,该温度下pH=1的硫酸中c(H+)=0.1mol/L、pH=11的NaOH溶液中c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$mol/L=0.01mol/L,要使混合溶液呈中性,说明n(H+)=n(OH-),即0.01mol/L×aL=0.1mol/L×bL,a:b=10:1,
故答案为:大于;25℃时KW=10-14,升高温度水的电离平衡正向移动,使KW增大;10:1.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析判断及计算能力,明确溶液中离子浓度与pH的关系是解本题关键,知道温度对水电离平衡移动的影响原理,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-2Q2+Q3) kJ•mol-1 | |
| B. | S(s)+2CO(g)═SO2(g)+2C(s)△H=(Q1-Q3) kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(Q1-2Q2+Q3) kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-Q2+2Q3) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不是在室温下 | B. | 弱酸溶液与强碱溶液反应 | ||
| C. | 强酸溶液与强碱溶液反应 | D. | 二元强酸溶液和一元强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
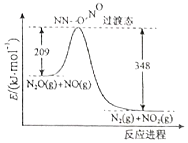 请完成下列问题
请完成下列问题| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 向稀盐酸溶液中加入铁粉:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| D. | 向AlCl3溶液中加入过量的氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、K+、OH-、NO3-、CO32-、SO42-.为了进一步确认,对该溶液进行实验检测:
某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、K+、OH-、NO3-、CO32-、SO42-.为了进一步确认,对该溶液进行实验检测:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ③⑤⑥ | C. | ①②④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32 g O3含有的氧原子数目为2NA | |
| B. | 5.6 g的Fe在足量Cl2中完全燃烧转移电子数为0.2NA | |
| C. | 0.1 mol•L-1 Na2SO4溶液含有的钠离子数目为0.2NA | |
| D. | 标准状况下,22.4 L苯含有的碳原子数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com