
生物质能来源于植物及其加工产品所贮存的能量,是人类赖以生存的重要能源。下列有关叙述不正确的是( )
A.绿色植物通过光合作用,将化学能转化为生物质能
B.农村通过杂草和动物的粪便发酵制沼气,沼气的主要成分是甲烷
C.推广使用乙醇汽油,乙醇可由富含淀粉的农作物发酵产生
D.开发生物质能有利于环境保护和经济可持续发展
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:A(g)+2B(g)2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2)K和x的关系满足K=__________。在保证A浓度不变的情况下,扩大容器的体积,平衡______(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
(3)该反应的逆反应速率与时间的关系如图所示。
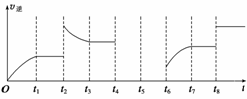
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时________________________________________________________________________;
t8时________________________________________________________________________。
②t2时平衡向______(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
查看答案和解析>>
科目:高中化学 来源: 题型:
进行下面的实验要用到下列一种或几种仪器,请用这些仪器的名称填空。
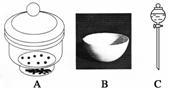
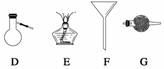
(1)欲干燥NH3需使用仪器________________________________________________;
(2)欲分离互不相溶的两种液体,可使用____________________________________;
(3)欲分离液态混合物中沸点不同的组分,可使用_____________________________;
(4)欲分离悬浮于液体中的固体物质,可使用_________________________________;
(5)欲用胆矾晶体(CuSO4·5H2O)制无水硫酸铜固体,可使用:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
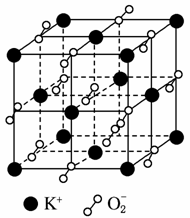
高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如右图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )
A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O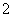
B.晶体中每个K+周围有8个O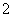 ,每个O
,每个O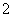 周围有8个K+
周围有8个K+
C.晶体中与每个K+距离最近的K+有8个
D.晶体中,0价氧与-2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.高温太阳炉是把热能转变成电能的过程
B.化石燃料燃烧时放出的能量来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.食用植物体内的淀粉、蛋白质等属直接利用能源
查看答案和解析>>
科目:高中化学 来源: 题型:
太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下某种盐熔化,吸收热量,晚间熔盐固化释放出相应的能量,已知下表数据:
| 盐 | 熔点(℃) | 熔化吸热(kJ·mol-1) | 参考价格(元·t-1) |
| CaCl2·6H2O | 29.9 | 37.3 | 780~850 |
| Na2SO4·10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4·12H2O | 35.1 | 100.1 | 1 600~2 000 |
| Na2S2O3·5H2O | 45.0 | 49.7 | 1 400~1 800 |
其中最适宜选用作为储能介质的是( )
A.CaCl2·6H2O B.Na2SO4·10H2O
C.Na2HPO4·12H2O D.Na2S2O3·5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是( )
A.葡萄糖和麦芽糖都溶于水、有甜味
B.麦芽糖的相对分子质量是葡萄糖的两倍
C.淀粉和纤维素的相对分子质量不同,但所含碳、氢、氧的质量比相同
D. 1 mol麦芽糖完全水解生成2 mol葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
现有电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2 ④CH3COONa ⑤NaOH,且已知:CO2+3H2O+2AlO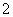 ===2Al(OH)3↓+CO
===2Al(OH)3↓+CO 。
。
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是__________________。
(2)将上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,其pH变化最大的是________(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,有气体产生的是________(填编号)。
(4)将上述①②③④四种电解质溶液混合时,发生反应的离子方程式为_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com