
下列递变规律不正确的是( )
A. Na、Mg、Al还原性依次减弱
B. I2、Br2、Cl2氧化性依次增强
C. C、N、O原子半径依次增大
D. P、S、Cl最高正价依次升高
科目:高中化学 来源:2017届黑龙江哈尔滨三中高三上期中化学试卷(解析版) 题型:选择题
在t ℃下,某反应达到平衡,平衡常数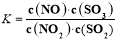 。恒容时,
。恒容时, 温度升高,NO浓度减小。下列说法正确的是
温度升高,NO浓度减小。下列说法正确的是
A.该反应正反应的焓变为正值
B.恒温下扩大容器体积,反应体系的颜色加深
C.升高温度,逆反应速率减小
D.该反应化学方程式为NO2+SO2 NO+SO3
NO+SO3
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上月考三化学试卷(解析版) 题型:选择题
用电解水的方法分析水的组成时,需要加入一些电解质以增强水的导电性,不宜加入的物质是( )
A.Na2SO4 B.NaNO3 C.KOH D.CuSO4
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上月考三化学试卷(解析版) 题型:选择题
已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1 mol/L NaHSO3和NaHCO3的两种溶液,两种溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中正确的一组是 ( )
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(H+)+c(H2RO3)=c(HRO3-)+c(OH-)
C.c(Na+)+c(H+)=c(HRO3-)+2c(RO32-)+c(OH-)
D.两溶液中c(Na+)、c(HRO3-)、 c(RO32-) 分别相等
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上月考三化学试卷(解析版) 题型:选择题
下列表示的是异丙基的是( )
A.CH3CH2CH3
B.CH3CH2CH2﹣
C.﹣CH2CH2CH2﹣
D.(CH3)2CH﹣
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上月考二化学卷(解析版) 题型:填空题
(1)实验室用Na2CO3?10H2O晶体配制0.05mol/L的Na2CO3溶液970mL,应选用的容量瓶的规格 ,称取Na2CO3?10H2O的质量是 g。
(2)2molO3和3molO2的质量之比为 ,分子数之比为 ,同温同压下的密度之比为 ,含氧原子数之比为 。
(3)现有下列九种物质①AgCl ②铜 ③液态醋酸 ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦酒精 ⑧稀硝酸 ⑨熔融FeCl3
①上述状态下可导电的是(填序号,下同) ,属于电解质的是 ,属于非电解质的是 。
②上述九种物质中有两种物质之间可发生离子反应H++OH-=H2O,该离子反应对应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中选修化学卷(解析版) 题型:填空题
原子序数依次增大的X、Y、Z、W四种元素,X、Z基态原子的2p原子轨道上均有2个未成对电子, W基态原子的除第四层只有1个电子外,其余内层均为全满结构。
W基态原子的除第四层只有1个电子外,其余内层均为全满结构。
(1)W基态原子的价电子排布式为 。元素X、Y、Z的第一电离能由小到大顺序是 (填元素符号)。
(2)与XYZ-互为等电子体的一种分子为 (填化学式)。
(3)1 mol H2XZ3分子中含有σ键的数目为 。
(4)YH3极易 溶于水的主要原因是 。
溶于水的主要原因是 。
(5)尿素(H2NCONH2)可用于制有机铁肥,主要代表有 [Fe(H2NCONH2)6](NO3)3 [三硝酸六尿素合铁(Ⅲ)]。
①尿素分子中C、N原子的杂化方式分别是 。
②[Fe(H2NCONH2)6](NO3)3中“H2NCONH2”与Fe(Ⅲ)之间的作用力是 。根据价层电子对互斥理论推测NO3—的空间构型为 。

(6)CO2和NH3是制备尿素的重要原料,固态CO2(干冰)的晶胞结构如图所示。
①1个CO2分子周围等距离且距离最近的CO2分子有 个。
②铜金合金的晶胞结构与干冰相似,若顶点为Au、面心为Cu,则铜金合金晶体中Au与Cu原子数之比为是 。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上期中化学试卷(解析版) 题型:填空题
合成氨工业上常用下列方法制备H2 :
:
方法①:C(s)+2H2O(g) CO2(g)+2H2(g)
CO2(g)+2H2(g)
方法②:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知①C(石墨)+O2(g)═CO2(g)△H=-394kJ•mol-1
②2C(石墨)+O2(g)═2CO2(g)△H=-222kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
试计算25℃时由方法②制备1000gH2所放出的能量为_________kJ。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:
C(s)+2H2O(g) CO2(g)+2H2(g)其相关数据如下表所示:
CO2(g)+2H2(g)其相关数据如下表所示:

①T1_________T2(填“>”、“=”或“<”);
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度范围是____________。
③在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_________。
A.V逆(CO2)=2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均摩尔质量保持不变
④某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
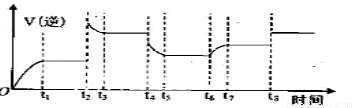
在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是_____________,从t1到t8哪个时间段H2O(g)的平衡转化率最低____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com