
【题目】已知2Fe2++Br2=2Fe3++2Br﹣ . 向100mL的FeBr2溶液中通入标准状况下的Cl23.36L,充分反应后测得溶液中Cl﹣与Br﹣的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
A.2 mol/L
B.1 mol/L
C.0.4 mol/L
D.0.2 mol/L
【答案】A
【解析】解:还原性Fe2+>Br﹣,通入氯气先发生反应2Fe2++Cl2═2Fe3++2Cl﹣,Fe2+反应完毕,剩余的氯气再发生反应2Br﹣+Cl2═Br2+2Cl﹣,反应后溶液中Cl﹣和Br﹣ 的物质的量浓度相等,说明氯气完全反应,Cl2的物质的量= ![]() =0.15mol,若Br﹣没有反应,n(Br﹣)=0.3mol,则n(FeBr2)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2,故有部分Br﹣参加反应,
=0.15mol,若Br﹣没有反应,n(Br﹣)=0.3mol,则n(FeBr2)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2,故有部分Br﹣参加反应,
设FeBr2的物质的量为x,则n(Fe2+)=x mol,n(Br﹣)=2x mol,未反应的n(Br﹣)=0.3 mol,参加反应的n(Br﹣)=(2x﹣0.3)mol,根据电子转移守恒有x×1+[2x﹣0.3]×1=0.15mol×2,解得x=0.2 mol,所以原FeBr2溶液的物质的量浓度为 ![]() =2mol/L.
=2mol/L.
故选:A.


科目:高中化学 来源: 题型:
【题目】在一定温度下,固定容积的容器中加入a mol A和b mol B,发生反应:A(g)+2B(g)2C(g)一段时间后达到平衡,生成n mol C.则下列说法中不正确的是( )
A.再充入少量A,平衡向正反应方向移动,但K值不变
B.起始时刻和达到平衡后容器中的压强之比为(a+b):(a+b﹣ ![]() )
)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar)增大压强,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有KOH和Ca(OH)2的混合溶液,C(OH﹣)═0.1molL﹣1 . 取此溶液500mL,向其中通入CO2 , 通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( ) 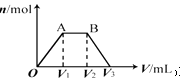
A.560、672
B.1008、1120
C.2240、2352
D.392、504
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3) 等等,其中硫酸最为重要,在工业上有广泛的应用,在实验室,浓硫酸是常用的干燥剂.
(1)焦硫酸(H2SO4SO3)溶于水,其中的SO3都转化为硫酸,若将890g焦硫酸溶于水配成8.00L硫酸,该硫酸的物质的量浓度=molL﹣1;
(2)若以浓硫酸吸水后生成H2SO4H2O计算,500g质量分数为98%的硫酸能吸收水的质量= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni﹣Cd)可充电电池在现代生活中有广泛应用.电解质溶液为KOH溶液,电池反应为:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2 , 下列有关镍镉电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2 , 下列有关镍镉电池的说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.充电时阳极反应为Cd(OH)2+2e﹣═Cd+2OH ﹣
C.放电时电池内部OH﹣向正极移动
D.充电时与直流电源正极相连的电极上发生Ni(OH)2转化为NiO(OH)的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法正确的是( )
A.将饱和硫酸铜溶液降温,析出的固体不是晶体
B.假宝石往往是玻璃仿造的,可以用划痕的方法鉴别宝石和玻璃制品
C.石蜡和玻璃都是非晶体,但它们都有固定的熔点
D.蓝宝石在不同方向上的硬度一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁和稀硫酸制氢气,不能加快氢气生成速率的措施是
A. 用等质量的铁粉代替铁片B. 用98%浓硫酸代替稀硫酸
C. 在稀硫酸中滴加少量CuSO4溶液D. 溶液加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com