
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32? |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42? |
| C、加入氯水后再加入KSCN溶液,溶液变红色,一定有Fe2+ |
| D、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、797.5kJ/mol |
| B、900.5kJ/mol |
| C、962.5kJ/mol |
| D、1595kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下:
用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下:| 实验次数 | 起始滴定管读数 | 终点滴定管读数 |
| 1 | 0.00mL | 24.02mL |
| 2 | 0.50mL | 24.46mL |
| 3 | 1.00mL | 25.02mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
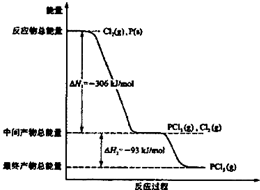 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(如图中的△H表示生成lmol产物的数据).
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(如图中的△H表示生成lmol产物的数据).查看答案和解析>>
科目:高中化学 来源: 题型:

| A、迷迭香酸的所含官能团为:羟基、羧基、酯基和苯环 |
| B、1mol迷迭香酸最多能和8mol H2发生加成反应 |
| C、迷迭香酸可以发生水解反应、取代反应和酯化反应 |
| D、1mol迷迭香酸最多能和含5mol Br2单质完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
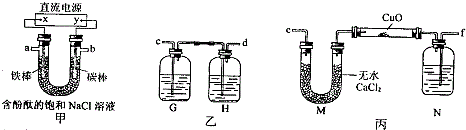
 某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).| 1 |
| 5 |
| 1 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、蒸发、蒸馏、过滤、萃取 |
| B、过滤、蒸馏、蒸发、萃取 |
| C、过滤、蒸发、蒸馏、分液 |
| D、蒸馏、蒸发、过滤、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com