
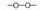 ,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)
,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)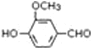 )可用于合成青蒿素,合成天然香草醛的反应如图:
)可用于合成青蒿素,合成天然香草醛的反应如图: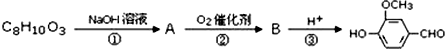
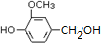 .
.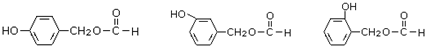 .
.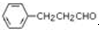 是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).
是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).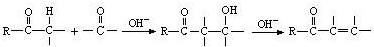
分析 (1)键线式中交点、端点为碳原子,用氢原子饱和碳的四价结构;
(2)在有机合成中引入羟基,可以通过卤代烃的取代、醛与氢气的加成也是还原等方法,不能通过酯化和消去反应得到;
(3)(4)根据C8H10O3的分子式中知,其不饱和度为4,根据 的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为
的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为 ,与氢氧化钠反应生成A为
,与氢氧化钠反应生成A为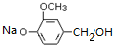 ,A发生催化氧化生成B为
,A发生催化氧化生成B为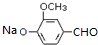 ,B再酸化得
,B再酸化得 ;
;
(5)C与 互为同分异构体,C符合下列条件:①苯环二取代,②能水解,说明含有酯基,③能发生银镜反应,说明含有醛基,结合②可知含有甲酸形成的酯基;④与FeCl3溶液发生显色反应,说明含有酚羟基;
互为同分异构体,C符合下列条件:①苯环二取代,②能水解,说明含有酯基,③能发生银镜反应,说明含有醛基,结合②可知含有甲酸形成的酯基;④与FeCl3溶液发生显色反应,说明含有酚羟基;
(6)由苯甲醛和氯乙烷为原料,制备苄基乙醛可以用氯乙烷碱性水解得乙醇,再氧化得乙醛,乙醛与苯甲醛在碱性条件下发生信息中的反应得到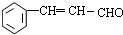 ,再与氢气催化加成即可得到苄基乙醛.
,再与氢气催化加成即可得到苄基乙醛.
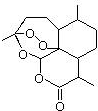
解答 解:(1)根据青蒿素的结构简式可知其分子式为C15H22O5,
故答案为:C15H22O5;
(2)在有机合成中引入羟基,可以通过卤代烃的取代、醛与氢气的加成也是还原等方法,不能通过酯化和消去反应得到,故选:①②⑤;
(3)根据C8H10O3的分子式中知,其不饱和度为4,根据 的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为
的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为 ,与氢氧化钠反应生成A为
,与氢氧化钠反应生成A为 ,A发生催化氧化生成B为
,A发生催化氧化生成B为 ,B再酸化得
,B再酸化得 .
.
根据上面的分析可知,步骤①③的作用是保护酚羟基,避免被氧化,
故答案为:保护酚羟基,避免被氧化;
(4)由(3)酯基分析可知,C8H10O3的结构简式为 ,
,
故答案为: ;
;
(5)C与 互为同分异构体,C符合下列条件:①苯环二取代,②能水解,说明含有酯基,③能发生银镜反应,说明含有醛基,结合②可知含有甲酸形成的酯基;④与FeCl3溶液发生显色反应,说明含有酚羟基,则符合条件的C的结构简式为:
互为同分异构体,C符合下列条件:①苯环二取代,②能水解,说明含有酯基,③能发生银镜反应,说明含有醛基,结合②可知含有甲酸形成的酯基;④与FeCl3溶液发生显色反应,说明含有酚羟基,则符合条件的C的结构简式为: ,
,
故答案为: ;
;
(6)由苯甲醛和氯乙烷为原料,制备苄基乙醛可以用氯乙烷碱性水解得乙醇,再氧化得乙醛,乙醛与苯甲醛在碱性条件下发生信息中的反应得到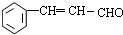 ,再与氢气催化加成即可得到苄基乙醛,合成路线流程图为:
,再与氢气催化加成即可得到苄基乙醛,合成路线流程图为: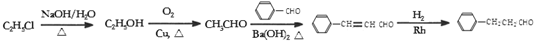 ,
,
故答案为: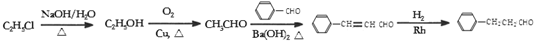 .
.
点评 本题考查有机物推断与合成、有机物的结构、限制条件同分异构体书写、官能团的性质与衍变等,是对有机化学基础的综合考查,难度中等.


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:填空题
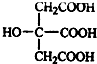 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
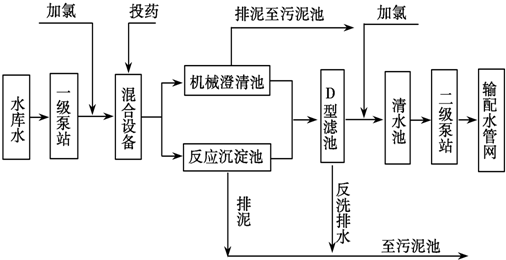
| A. | 若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池 | |
| B. | 投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3-等 | |
| C. | 自来水生产中,前面加氯起消毒杀菌作用,后面加氯是保持水中有效氯的含量,防止自来水二次污染 | |
| D. | 用ClO2消毒自来水,消毒效率是等质量氯气的2.63倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ”和画“×”分别标明B和N的相对位置.
”和画“×”分别标明B和N的相对位置.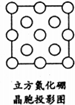
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “地沟油”禁止食用,但可以用来制肥皂 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 | |
| D. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCH3+(甲基碳正离子)含有的电子数目为9NA | |
| B. | 27g Al在标准状况下的22.4L Cl2中燃烧,转移的电子总数为3 NA | |
| C. | 0.2 mol•L-1的Na2CO3溶液中含有CO32-的数目一定小于0.2NA | |
| D. | 7.8gNa2S和Na2O2的混合物中含有的阴离子总数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

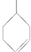 .
.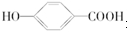 在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式)
在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) .
.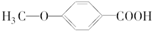 的同分异构体很多,其中符合下列条件的有3种.
的同分异构体很多,其中符合下列条件的有3种. .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 相关信息 |
| X | X的最高价氧化为对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
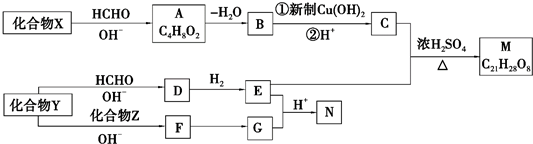
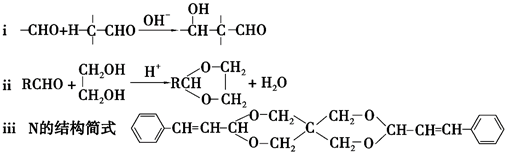
 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$ +Cu2O↓+3H2O.
+Cu2O↓+3H2O. .
.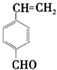 和
和 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com