
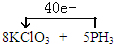 ,PH3是还原剂,若有1mol 还原剂PH3被氧化转移电子8mol,故答案为:8.
,PH3是还原剂,若有1mol 还原剂PH3被氧化转移电子8mol,故答案为:8.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
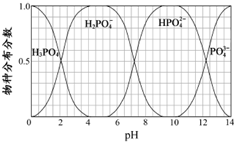
| 酸 | 电离常数(25℃) |
| HF | Ki=3.6×10 -4 |
H3PO4 | Ki1=7.5×10 -3 Ki2=6.2×10 -8 Ki3=2.2×10 -13 |
| A、NaF和H3PO4反应的产物只有HF、NaH2PO4 |
| B、0.10 mol/L的溶液,pH由大到小的顺序是Na3PO4>Na2HPO4>NaF>NaH2PO4 |
| C、0.10 mol/L的H3PO4溶液中,0.30 mol/L>c(H+)>0.10 mol/L |
| D、25℃时,等体积、等浓度的NaF和NaH2PO4溶液中所含离子总数前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.01×1023个SO2分子的质量为32 g |
| B、CH4的摩尔质量为16 g |
| C、1 mol H2O的质量为18 g/mol |
| D、不同的气体,若体积不等,则它们所含的分子数一定不等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
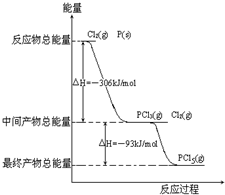
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氮元素可形成卤化物、叠氮化物及络合物等.
氮元素可形成卤化物、叠氮化物及络合物等.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 mL;21.2 g |
| B、500 mL;100.7 g |
| C、1000 mL;201.4 g |
| D、1 000 mL;212.0 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com