

| A. | 用装置甲验证在该条件下铁钉发生吸氧腐蚀 | |
| B. | 装置乙用于HCl的吸收,以防倒吸 | |
| C. | 用装置丙验证实验室制得的乙烯中混有二氧化硫和二氧化碳 | |
| D. | 关闭活塞a,从b处加水,以检查装置丁的气密性 |
分析 A.水为中性,Fe发生吸氧腐蚀;
B.HCl易溶于水,倒置的烧瓶可防止倒吸;
C.乙烯、二氧化硫均能被高锰酸钾氧化,二氧化硫、二氧化碳均能使石灰水变浑浊;
D.关闭活塞a,从b处加水,U型管左右两侧出现液面差可检验气密性.
解答 解:A.水为中性,Fe发生吸氧腐蚀,则装置甲可验证在该条件下铁钉发生吸氧腐蚀,故A正确;
B.HCl易溶于水,倒置的烧瓶可防止倒吸,则装置乙用于HCl的吸收,以防倒吸,故B正确;
C.乙烯、二氧化硫均能被高锰酸钾氧化,二氧化硫、二氧化碳均能使石灰水变浑浊,则该装置不能验证实验室制得的乙烯中混有二氧化硫和二氧化碳,应选通过品红检验二氧化硫,再通过高锰酸钾,最后利用石灰水检验二氧化碳,故C错误;
D.关闭活塞a,从b处加水,若U型管左右两侧出现液面差,可检验气密性良好,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握化学反应原理、实验装置的作用、实验技能为解答的关键,侧重学生的分析、实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
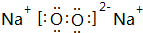
| A. | 羟基的电子式: | B. | 石炭酸的结构简式:C6H5OH | ||
| C. | 乙醛的分子式:C2H4O | D. | 酚醛树脂的结构简式为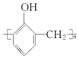 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Al3+、NH4+、Cl-、S2- | |
| B. | 由水电离得到的c(H+)=1×10-13mol•L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 0.1 mol•L-1NH4HCO3溶液中:K+、Na+、AlO2-、Cl- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | O | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;| 危险性 |  |
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NF3既是氧化剂,又是还原剂 | |
| B. | 还原剂与氧化剂的物质的量之比为1:2 | |
| C. | 若生成2molHNO3,则转移2mol电子 | |
| D. | NF3中氮元素的化合价为+3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com