
分析 (1)氧化还原反应中的,化合价升高值=化合价降低值=转移电子数目;化合价升高的元素被氧化,化合价降低的元素所在的反应物是氧化剂,据此回答;
(2)被还原的硝酸生成NO,根据氮原子守恒n被还原(HNO3)=n(NO),根据关系式3Cu~2NO~2HNO3计算.
解答 解:(1)该氧化还原反应中的,化合价升高的是铜元素,化合价降低的是硝酸中的氮元素,转移电子数为6mol,双线桥法表示电子转移的方向和数目如下所示: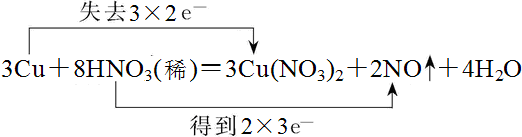 ,
,
故答案为: ;
;
(2)被还原的硝酸生成NO,根据氮原子守恒n被还原(HNO3)=n(NO),则:
3Cu~2NO~2HNO3
3×64 2×63
19.2g m(HNO3)
则m(HNO3)=$\frac{19.2g×2×63}{3×64}$=12.6g
答:被还原的HNO3的质量为12.6g.
点评 本题考查了氧化还原反应电子转移和氧化还原反应的计算,难度中等,本题采取关系式计算,也可以利用电子转移守恒计算.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 的系统命名是:2,6-二甲基辛烷
的系统命名是:2,6-二甲基辛烷 的键线式是
的键线式是
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,回答下列问题:
,回答下列问题: $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +2H2O.
+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 31.00 |
| 2 | 20.00 | 1.00 | 32.04 |
| 3 | 20.00 | 1.10 | 32.18 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;C中所含官能团的名称是羧基、溴原子.
;C中所含官能团的名称是羧基、溴原子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 石墨烯是一种有机物 | B. | 石墨烯中碳原子间以共价键结合 | ||
| C. | 石墨烯具有和乙烯相同的性质 | D. | 12g石墨烯中约含6.02×1023个e- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com