
| A. | 标准状况下,22.4LCCl4含有的分子数约为6.02×1023个 | |
| B. | 1L氢气一定比1L氧气质量少 | |
| C. | 含有6.02×1023个Fe3+的Fe2(SO4)3中SO42-的物质的量为3mol | |
| D. | 1molAl3+带有的正电荷数为3NA |
分析 A.标准状况下,CCl4为液体;
B.状态不知道,无法计算气体的物质的量和质量;
C.根据n=$\frac{N}{{N}_{A}}$计算Fe3+的物质的量,由化学式可知n(SO42-)=$\frac{3}{2}$n(Fe3+);
D.根据Al3+中正电荷数计算.
解答 解:A.标准状况下,CCl4为液体,不能用气体摩尔体积计算,故A错误;
B.状态不知道,无法计算气体的物质的量和质量,所以不能比较氢气和氧气的质量大小,故B错误;
C.Fe3+的物质的量为$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1mol,由化学式可知n(SO42-)=$\frac{3}{2}$n(Fe3+)=1mol×$\frac{3}{2}$=1.5mol,故C错误;
D.1molAl3+带有的正电荷的物质的量为3mol,则正电荷数为3NA,故D正确.
故选D.
点评 本题考查了物质的量有关计算,题目难度不大,注意把握气体摩尔体积的适用条件、微粒之间的数目关系,侧重于考查学生的分析能力和计算能力.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:选择题
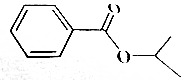 某有机物结构如图所示,有关该物质的叙述正确的是( )
某有机物结构如图所示,有关该物质的叙述正确的是( )| A. | 该物质易溶于水,不溶于乙醇、乙醚 | |
| B. | 该物质能发生加成、氧化.水解等反应 | |
| C. | 1mol该物质最多能与4mol氢气加成 | |
| D. | 该物质所有碳原子可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 | |
| X | 中和反应 | 无现象 | 溶解 | 产生氢气 |
| Y | 无现象 | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| Z | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | 无现象 |
| W | 水解反应 | 无现象 | 无现象 | 无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用右图所示装置除去含CN-、CI-废水中的CN-时,控制溶液pH为9-10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
用右图所示装置除去含CN-、CI-废水中的CN-时,控制溶液pH为9-10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )| A. | 用石墨作阳极,铁作阴极 | |
| B. | 阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O | |
| C. | 阴极的电极反应式为:2H++2e-=H2↑ | |
| D. | 除去CN-的反应:2CN-+5ClO-+2H+═N2↑+2CO2↑+5Cl-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 | |
| B. | 《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐 | |
| C. | 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 | |
| D. | 《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com