
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面判断.
解答 解:(1)CH3CH2CH═CH2为1-丁烯,相当于乙烯中的1个H被乙基取代后得到的产物,处于乙烯基的2个C和3个H共平面,乙基中的1个C与乙烯基共平面;
(2)CH2═CH-CH═CH2为1,3-丁二烯,为两个乙烯基结构,所有原子可以共平面;
(3)C6H5-C≡CH为苯乙炔,乙炔为直线形结构,苯为平面结构,所有原子可以共平面;
(4)CH3CH═CH2为丙烯,相当于乙烯中的1个H被甲基取代生成的产物,乙烯基与甲基中的C可以共平面.
答:(1)乙烯基的2个C和3个H共平面,乙基中的1个C与乙烯基共平面;
(2)所有原子共平面;
(3)所有原子共平面;
(4)3个C与3个H共平面.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.


科目:高中化学 来源: 题型:选择题
| A. | 分子组成相差一个或若干个CH2原子团的化合物一定互为同系物 | |
| B. | 互为同分异构体的有机物的组成元素相同,但结构必须不同 | |
| C. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| D. | 互为同系物的有机物其相对分子质量数值一定相差14n(n为正整数) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
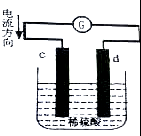 如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )| A. | d为负极,电池工作时,d极发生氧化反应 | |
| B. | c为锌片,电池工作时,溶液中SO42-向c极移动 | |
| C. | 电池工作的过程中,d电极上产生大量的气泡 | |
| D. | 电池工作的过程中,溶液的pH基本不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
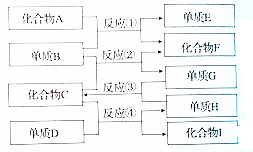
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 7:8 | D. | 8:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②①③④⑤ | B. | ①②③④⑤ | C. | ②③①④⑤ | D. | ③②①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 基态原子M层全充满,N层只有一个电子 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com