
下列关于乙烯和聚乙烯的叙述不正确的是
A.乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物
B.乙烯的化学性质比聚乙烯活泼
C.取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等
D.取等物质的量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的物质的量分别相等
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年四川成都七中高一下课后作业乙烯化学试卷(解析版) 题型:实验题
下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各小题。

(1)碎瓷片的作用是_____________。
(2)B中现象是________,乙烯发生_______反应。
(3)C中现象是________,发生反应的化学方程式______________________。
(4)在D处点燃时必须进行的操作是___________________________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省师大一附高三5月月考理综化学试卷(解析版) 题型:实验题
硫酸亚铁晶体(FeSO4· 7H2O)俗称绿矾,加热至高温会分解。某化学研究小组利用下列装置探究FeSO4分解后的产物。
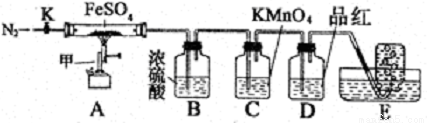
实验步骤:
按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取mgFeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K。加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃。待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末。请回答下列问题:
(1)仪器甲的名称是__________;
(2)B中浓硫酸的作用__________。
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化。写出C中发生反应的离子方程式__________;
(4) FeSO4完全分解后,还需要通入一段时间N2的原因是__________。
(5)若C中原先加入了20mL 1.00mol/L的KMnO4溶液,为了确定FeSO4分解的化学方程式,某同学进行了如下实验:
Ⅰ、称量B装置在实验前后增重 0.80g;
Ⅱ、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
Ⅲ、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mo1/L标准H2C2O4溶液滴定至终点:
Ⅳ、重复实验3次.记录数据如下:
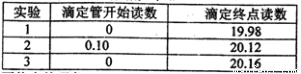
①滴定至终点的现象__________。
②FeSO4分解的化学方程式为__________。
(6)请设计一个实验来检验A中的FeSO4是否完全分解__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期中化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
①、CH3—CH=CH2和CH2=CH2的最简式相同 ②、CH≡CH和C6H6含碳的质量分数相同③、环己烷和戊烷互为同系物 ④、正戊烷、异戊烷、新戊烷的沸点逐渐变低⑤、标准状况下,11.2L的戊烷所含的分子数为0.5 NA (NA为阿伏加德罗常数)
A.① ② B.③ ④ C.② ③ D.③ ⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期中化学试卷(解析版) 题型:选择题
X、Y和Z三种短周期元素,原子序数之和为32,X和Y为相邻周期的元素,Y和Z为相同周期的元素。Y的质子数比X多5个,X的最外层电子数为Y的最外层电子数的2倍,X的最外层电子数和Z的最外层电子数之和为7,下列叙述中不正确的是 ( )
A.X和Y两种元素构成一种阴离子,该阴离子与强酸反应时,可能变成Y的阳离子
B.元素Y的最高价氧化物能溶于Z的最高价氧化物的水化物中
C.X、Y和Z三元素组成的化合物为碱
D.X与Z的单质在不同条件下能生成不同的化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期中化学试卷(解析版) 题型:选择题
2012年5月30日,国际理论(化学)与应用化学联合会(IUPAC)正式接受114,116两种新元素。元素114号命名为flerovium(Fl),以纪念苏联原子物理学家乔治·弗洛伊洛夫,下列关于114号元素的下列说法正确的是( )
A.114号元素的质量数为114 B.114号元素是过渡元素
C.114号元素是非金属元素 D.114号元素原子最外层有4个电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期中化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
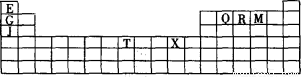
(1)写出基态T3+的核外电子排布式: ;T在周期表中所在分区为 。
(2)Q、R、M的第一电离能由大到小的顺序是 (用元素符号表示),原因 。
(3)下列有关上述元素的说法正确的是 。
A.J比X活泼,所以J可以在溶液中置换出X
B.将J2M2溶于水,要破坏离子键和共价键
C.RE3沸点高于QE4,主要是因为前者相对分子质量较大
D.一个Q2E4分子中含有五个δ键和一个π键
(4)G2O的熔点比J2O的 (填“高”或“低”) ,其原因是 。
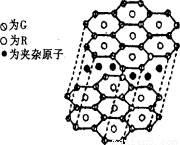
(5) G与R单质直接化合生成一种离子化合物G3R。该晶体具有类似石墨的层状结构。每层中,G原子构成平面六边形,每个六边形的中心有一个R原子。层与层之间还夹杂一定数量的原子。请问这些夹杂的原子应该是 (填G或R的元素符号)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期中化学试卷(解析版) 题型:选择题
如图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )
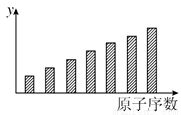
A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是形成基态离子转移的电子数
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下第一次月考化学试卷(解析版) 题型:选择题
用VSEPR模型预测下列分子或离子的立体结构,其中正确的是( )
A.H2O与BeCl2为角形(V形) B.CS2与SO2为直线形
C.BF3与PCl3为三角锥形 D.SO3与CO32-为平面三角形
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com