
科目:高中化学 来源: 题型:单选题
铅蓄电池的反应原理为:2PbSO4+2H2O Pb+PbO2+2H2SO4,下列叙述中,正确的是
Pb+PbO2+2H2SO4,下列叙述中,正确的是
| A.PbSO4的氧化性比PbO2的强、还原性比Pb的强 |
| B.放电时,PbO2为氧化剂、做负极,Pb为还原剂、做正极 |
| C.放电时,当有2 mol H2SO4反应时,会有1.204×1024个电子从铅电极流出 |
| D.充电时,PbSO4既被氧化又被还原,Pb是阳极产物之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是
装置① 装置② 装置③
| A.装置①研究的是电解CuCl2溶液,b电极上有红色固体析出 |
| B.装置②研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e- = Fe2+ |
| C.装置③研究的是电解饱和食盐水, B电极发生的反应:2Cl--2e- = Cl2↑ |
| D.三个装置中涉及的主要反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
锌锰干电池在放电时总反应方程式可以表示为:Zn(s)+2MnO2+2N Zn2++Mn2O3(s)+2NH3↑+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
Zn2++Mn2O3(s)+2NH3↑+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
| A.Zn | B.碳 | C.MnO2和N | D.Zn2+和NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是( )
| A.X和Y与电流表连接,电子由Cu极流向Zn极 |
| B.X和Y与电流表连接,将Zn换成Fe测得电流更大 |
| C.X和Y分别与电源“-”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“-”、“+”极相连,Zn极质量减轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体。这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体。目前固体电解质在制造全固态电池及其他传感器、探测器等方面的应用日益广泛。如RbAg4I5晶体,其中迁移的物种全是Ag+,室温导电率达0. 27 Ω-1·cm-1。利用RbAg4I5晶体,可以制成电化学气敏传感器。下图是一种测定O2含量的气体传感器示意图,被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是( )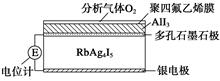
| A.I2+2Rb++2e-=2RbI |
| B.I2+2Ag++2e-=2AgI |
| C.Ag-e-=Ag+ |
| D.4AlI3+3O2=2Al2O3+6I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min 间的平均反应速率和推测反应16 min 时反应物的浓度,结果应是( )。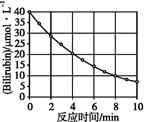
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )。
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的酸性均减弱 |
| D.产生气泡的速率甲比乙慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示。下列有关叙述正确的是 ( )。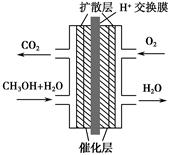
| A.通氧气的一极为负极 |
| B.H+从正极区通过交换膜移向负极区 |
| C.通甲醇的一极的电极反应式为CH3OH+H2O-6e-=CO2↑+6H+ |
| D.甲醇在正极发生反应,电子经过外电路流向负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com