
| A、不能与KOH反应 |
| B、能和稀硫酸反应放出无色无味刺激性气味 |
| C、治疗胃酸过多的一种药剂 |
| D、在其水溶液中加入石灰水有白色沉淀产生 |


科目:高中化学 来源: 题型:
| A、相同质量的Na2CO3和NaHCO3与足量盐酸作用时,碳酸氢钠反应速率更快,产生的气体质量相同 |
| B、NaHCO3俗名:小苏打.Na2CO3俗名:大苏打 |
| C、Na2CO3和NaHCO3均可与澄清石灰水反应 |
| D、Na2CO3和NaHCO3均可与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响 |
| B、在酸碱中和滴定实验中,滴定管都需润洗,否则引起误差 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
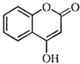 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: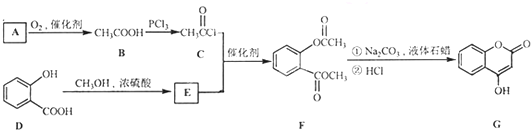
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,4.6g NO2含有0.2NA个氧原子 |
| B、0.1mol Na2O2固体中含有离子总数为0.4NA |
| C、标准状况下2.24L Cl2与足量的铁充分反应,转移电子数为0.3NA |
| D、等物质的量的NO和CO2所含分子数均为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在一定温度下,AgBr水溶液中c(Br-)和c(Ag+)的乘积是一个常数 |
| B、AgBr水溶液的导电能力很弱,所以AgBr为弱电解质 |
| C、室温下,AgBr在纯水中的溶解度大于在KBr溶液中的溶解度 |
| D、向饱和AgBr悬浊液中加入盐酸c(Br-)增大,Ksp值变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
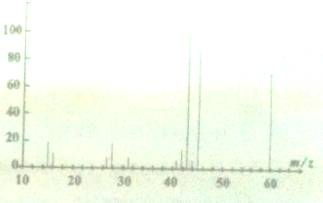
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度 |
| B、缩小容器体积 |
| C、增大容器体积 |
| D、降低温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com