
 2 CO32— + 6H2O,则下列说法错误的是
2 CO32— + 6H2O,则下列说法错误的是| A.充电时电解质溶液的pH逐渐增大 |
| B.放电时CH3OH参与反应的电极为正极 |
| C.充电时每生成1 mol CH3OH转移6 mol电子 |
| D.放电时负极的电极反应为:CH3OH-6e- +8OH- =CO32—+ 6H2O |
 2CO32-+6H2O,生成大量的氢氧根离子,所以碱性增强,故电解质溶液的pH逐渐增大,故A正确;
2CO32-+6H2O,生成大量的氢氧根离子,所以碱性增强,故电解质溶液的pH逐渐增大,故A正确; 2CO32-+6H2O,则放电时CH3OH参与反应的电极为负极,故B错误;
2CO32-+6H2O,则放电时CH3OH参与反应的电极为负极,故B错误; 2CO32-+6H2O,每生成2molCH3OH转移12mol电子,则每生成1mol
2CO32-+6H2O,每生成2molCH3OH转移12mol电子,则每生成1mol 2CO32-+6H2O,则负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O,故D正确。
2CO32-+6H2O,则负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O,故D正确。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源:不详 题型:填空题

| A.负极的电极反应式为:CO+O2-―2e=CO2 |
| B.工作时电极b作正极,O2-由电极a流向电极b |
| C.工作时电子由电极a通过传感器流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
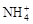 +2e-=Mn2O3+2NH3+H2O。
+2e-=Mn2O3+2NH3+H2O。| A.干电池中锌筒为正极,石墨棒为负极 |
| B.干电池工作时,电流方向是由锌筒经外电路流向石墨棒 |
| C.干电池长时间连续工作后,糊状物可能流出,腐蚀用电器 |
| D.干电池可实现化学能与电能的相互转化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Pb为正极被氧化 | B.溶液的pH不断减小 |
| C.SO42-只向PbO2处移动 | D.电解质溶液pH不断增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
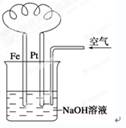
| A.这是电解NaOH溶液的装置 |
| B.溶液中发生了变化:4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| C.Fe为正极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
| D.NaOH溶液的碱性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
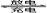 2Pb2++2H2O。若充放电过程中电解质溶液的体积变化忽略不计,下列有关新型液流式铅酸蓄电池的说法正确的是
2Pb2++2H2O。若充放电过程中电解质溶液的体积变化忽略不计,下列有关新型液流式铅酸蓄电池的说法正确的是| A.充放电时,溶液中Pb2+浓度保持不变 |
| B.充放电时,溶液的导电能力变化不大 |
| C.充电时,阳极反应式为:Pb2++2H2O-2e-=PbO2+4H+ |
| D.充电时,铅酸蓄电池的负极与外接电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |

 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1 CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1 CH3OCH3(g) + CO2 (g)的ΔH=
CH3OCH3(g) + CO2 (g)的ΔH= 
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
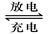 2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.MnO2发生了氧化反应 |
| B.MnOOH中Mn元素的化合价为+3 |
| C.反应消耗 0.65gZn,有0.01 mol电子发生转移 |
| D.电池正极的反应为:Zn + 2 OH-–2e-===Zn(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com