
| A. | 重氢原子:${\;}_{1}^{2}$D | |
| B. | S2-的结构示意图: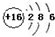 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | N2的电子式: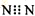 |
分析 A、21H原子俗称重氢原子;
B、硫离子是硫原子得2个电子后形成的;
C、质量数=质子数+中子数;
D、氮气中氮原子间有3对共用电子对.
解答 解:A、21H原子俗称重氢原子,质量数为2,质子数为1,故符号为21H,故A错误;
B、硫离子是硫原子得2个电子后形成的,故核外有18个电子,故结构示意图为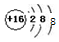 ,故B错误;
,故B错误;
C、质量数=质子数+中子数,故质子数为53,中子数为78的碘原子的质量数为131,符号为:${\;}_{53}^{131}$I,故C正确;
D、氮气中氮原子间有3对共用电子对,氮原子均达8电子稳定结构,故N2的电子式为: ,故D错误.
,故D错误.
故选C.
点评 本题考查了电子式的书写等常见的化学用语,题目难度中等,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
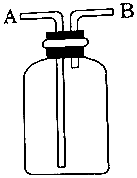
| A. | A瓶中盛满水,从B口进气,用排水法收集O2 | |
| B. | 瓶中盛适量浓硫酸,从A口进气来干燥Cl2 | |
| C. | 从B口进气,用排空气法收集Cl2 | |
| D. | 瓶中装满水,A口连导管并伸入量筒中,从B口进气,用排水法测量生成H2的大约体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| D. | 达到化学平衡时,正反应速率和逆反应速率都为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量 | |
| B. | O2前面的$\frac{1}{2}$表示参加反应的O2的分子数目 | |
| C. | 燃烧热是以在101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8 kJ•mol-1 | |
| D. | 1 mol H2和$\frac{1}{2}$ mol O2所具有的总能量大于1mol H2O(g)所具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com