
 4C��1��+2D( g)��ƽ��ʱ���n(C)="1.6mol" ,��Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ
4C��1��+2D( g)��ƽ��ʱ���n(C)="1.6mol" ,��Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ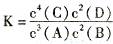

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g) ��H����92.4 kJ��mol-1������ʱ�� ��ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵������ȷ���ǣ� ��
2NH3(g) ��H����92.4 kJ��mol-1������ʱ�� ��ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵������ȷ���ǣ� ��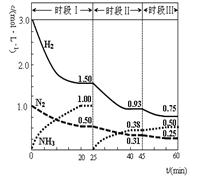
| A��ǰ20���ӷ�Ӧ�ڷų�������Ϊ46.2kJ |
| B����25���Ӹı�������ǽ�NH3�ӷ�Ӧ��ϵ�з����ȥ |
| C������60����ʱ��Ӧ�ִﵽ��ƽ�⣬��ʱ��ı�������ǽ����¶� |
| D��ʱ�������ʼͶ�ŵ�����Ũ������ԭ����2��,��Ӧ���ת��������,ƽ�ⳣ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 N2O4(g)����H��0����ƽ������������г���amolNO2���ٴδﵽƽ�����ԭƽ��Ƚϣ�������������ȷ����( )
N2O4(g)����H��0����ƽ������������г���amolNO2���ٴδﵽƽ�����ԭƽ��Ƚϣ�������������ȷ����( )| A��ƽ����Է����������� | B��NO2��ת������� |
| C��NO2�������������� | D����Ӧ�ų�������������ԭ����2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��5.4��10��5 | B��4.5��10��4 | C��0.015 | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3 (g)����H����197 kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��) 2 mol SO2��1 mol O2��(��) 1 mol SO2��0.5 mol O2��(��) 2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����
2SO3 (g)����H����197 kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��) 2 mol SO2��1 mol O2��(��) 1 mol SO2��0.5 mol O2��(��) 2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����| A��������ѹǿP��P����P�� > 2P�� |
| B��SO3������m��m����m�� > 2m�� |
| C��c(SO2)��c(O2)֮��k��k����k�� > k�� |
| D����Ӧ�ų���������������ֵQ��Q����Q�� > 2Q�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3�������淴Ӧ���ʿ��ø���Ӧ���������Ũ�ȵı仯��ʾ�����и���ϵ����˵����Ӧ�Ѵﵽƽ��״̬����
2NH3�������淴Ӧ���ʿ��ø���Ӧ���������Ũ�ȵı仯��ʾ�����и���ϵ����˵����Ӧ�Ѵﵽƽ��״̬����| A��3���� (N2)������ (H2) | B������ (N2)������ (NH3) |
| C��2���� (H2)��3���� (NH3) | D������ (N2)��3���� (H2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g)����H����92.4 kJ/mol]������˵����ȷ����
2NH3(g)����H����92.4 kJ/mol]������˵����ȷ����| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1 mol N2��3 mol H2 | 2 mol NH3 | 4 mol NH3 |
| NH3��Ũ��(mol/L) | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�a kJ | ����b kJ | ����c kJ |
| ��ϵѹǿ(Pa) | p1 | p2 | p3 |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ur- + H3O+ ��Ur- (aq)+Na+(aq)
Ur- + H3O+ ��Ur- (aq)+Na+(aq)  NaUr(s)
NaUr(s)| A����Ӧ�ġ�H>0 | B����Ӧ�ġ�H��0 |
| C�������¶�ƽ��������Ӧ�����ƶ� | D���ı��¶Ȳ�Ӱ��ƽ���ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO2��H>0���ܱ������з�Ӧ���ﵽƽ��״̬��Ҫʹ���������ɫ����ɲ�ȡ�ķ����� �ټ�Сѹǿ ����С����������¶Ȣ�����N2O4��Ũ�� �� ��
2NO2��H>0���ܱ������з�Ӧ���ﵽƽ��״̬��Ҫʹ���������ɫ����ɲ�ȡ�ķ����� �ټ�Сѹǿ ����С����������¶Ȣ�����N2O4��Ũ�� �� �� | A���ڢۢ� | B���٢ڢ� | C���٢ۢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com