
分析 (1)能导电的物质含有自由移动的电子或阴阳离子;电解质是指在水溶液中或熔融状态下能够导电的化合物,非电解质是指在熔融状态和水溶液中都不能导电的化合物,非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子,单质,混合物既不是电解质也不是非电解质;
(2)硫酸氢钠在水溶液中完全电离得到钠离子、氢离子、和硫酸根离子,一水合氨部分电离得到铵根离子和氢氧根离子.
解答 解:(1)①纯H2SO4,不能导电,溶于水能导电,是电解质;
②硝酸钾溶液,能导电,是混合物,既不是电解质也不是非电解质;
③铜,能导电,属于金属单质,既不是电解质也不是非电解质;
④二氧化碳,不能导电,属于非电解质;
⑤金刚石,是非金属单质,不能导电,既不是电解质也不是非电解质;
⑥硫酸氢钠固体,不能导电,溶于水或熔融状态下能导电,属于电解质;
⑦蔗糖,不能导电,是非电解质;
⑧NaI晶体,不能导电,溶于水或熔融状态下能导电,属于电解质;
⑨氨水,能导电,属于混合物,既不是电解质也不是非电解质;
⑩熔融KCl,能导电,是电解质,硫酸氢钠是酸式盐,在水溶液中电离出氢离子、钠离子和硫酸根离子,
故答案为:②③⑨⑩;①⑥⑧⑩;④⑦;
(2)硫酸氢钠在水溶液中完全电离得到钠离子、氢离子、和硫酸根离子,电离方程式为NaHSO4=Na++H++SO42-,
一水合氨部分电离得到铵根离子和氢氧根离子,电离方程式为NH3•H2O?NH4++OH-,
故答案为:NaHSO4=Na++H++SO42-;NH3•H2O?NH4++OH-.
点评 本题主要考查的是电解质与非电解质的概念以及能导电物质的判断,电离方程式的书写,难度不大,单质与混合物既不是电解质也不是非电解质,硫酸氢钠水溶液中的电离是易错点.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KMnO4作氧化剂 | |
| B. | 该反应不属于离子反应 | |
| C. | 氮元素被还原 | |
| D. | 当生成lmol MnSO4时,转移10 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水冲洗泄露的浓硫酸 | B. | 将熟石灰撒在泄露的浓硫酸上 | ||
| C. | 将氧化钡撒在泄露的浓硫酸上 | D. | 用土将泄露的浓硫酸掩埋 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2(s)+2C(s)═Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 | |
| B. | 一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | C(s)+H2O(g)?CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则CO2分解的热化学方程式为:2CO2(g)═2CO(g)+O2(g)△H=+283.0 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
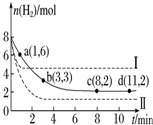 将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )
将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )| A. | 0.5mol•L-1•min-1. | B. | 0.1mol•L-1•min-1 | ||
| C. | 0 mol•L-1•min-1 | D. | 0.125mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物不存在 | B. | 该有机物的分子式为C4H4 | ||
| C. | 该有机物的空间构型为正四面体 | D. | 该有机物不属于笨的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com