
如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
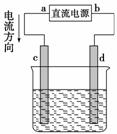
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
科目:高中化学 来源: 题型:
下列溶液中能够区别SO2和CO2气体的是 ( )
①澄清石灰水 ②H2S溶液 ③KMnO4酸性溶液 ④氯水 ⑤品红溶液
A.①②③ B.②③④ C.除①以外 D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关合成氨工业的叙述,可用勒·夏特列原理来解释的是( )
A.使用铁触媒,使N2和H2混合气体有利于合成氨
B.高压比常压条件更有利于合成氨的反应
C.500℃左右比室温更有利于合成氨的反应
D.合成氨时采用循环操作,可提高原料的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 mL 0.01 mol·L-1 KCl溶液中,加入1 mL 0.01 mol·L-1 AgNO3溶液,下列说法正确的是(AgCl的Ksp=1.8×10-10 mol2·L-2)( )
A.有AgCl沉淀析出 B.无AgCl沉淀
C.无法确定 D.有沉淀但不是AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
AgCl和Ag2CrO4的溶度积分别为1.8×10-10 mol2·L-2和2.0×10-12 mol3·L-3,若用难溶盐在溶液中的浓度来表示其溶解度,则下面的叙述中正确的是( )
A.AgCl和Ag2CrO4的溶解度相等
B.AgCl的溶解度大于Ag2CrO4的溶解度
C.两者类型不同,不能由Ksp的大小直接判断溶解能力的大小
D.都是难溶盐,溶解度无意义
查看答案和解析>>
科目:高中化学 来源: 题型:
在水中加等物质的量的Ag+、Pb2+、Na+、SO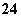 、NO
、NO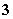 、Cl-,该溶液放在用惰性电极作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
、Cl-,该溶液放在用惰性电极作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
A.35.5∶108 B.16∶207 C.8∶1 D.108∶35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL (标准状况)气体。回答:
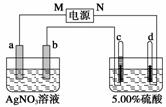
(1)直流电源中,M为__________极。
(2)Pt电极上生成的物质是________,其质量为__________________________g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为2∶______∶______∶________。
(4)AgNO3溶液的浓度________(填“增大”、“减小”或“不变”,下同),AgNO3溶液的pH______,硫酸的浓度__________________________,硫酸的pH________。
(5)若硫酸的质量分数由5.00%变为5.02%,则原有5.00%的硫酸________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
向某无色溶液中加入铁粉能产生大量H2,则该溶液中可能含有的能大量共存的离子组是( )
A.Na+、Ca2+、Cl-、NO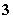
B.Fe3+、K+、Cl-、HCO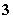
C.Cu2+、Na+、Cl-、SO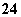
D.K+、Na+、Cl-、SO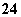
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com