
| A. | 燃烧反应 | B. | 铝热反应 | C. | 碳酸钙分解 | D. | 酸碱中和 |
分析 反应中反应物的总能量小于生成物的总能量,说明该反应为吸热反应,常见的吸热反应有:①氢氧化钡晶体与氯化铵晶体的反应,②大多数分解反应,③C、氢气或CO为还原剂的氧化还原反应等,以此解答该题.
解答 解:反应中反应物的总能量小于生成物的总能量,说明该反应为吸热反应,
A.燃烧为放热反应,故A不选;
B.铝热反应为放热反应,故B不选;
C.碳酸钙分解需要吸热,为吸热反应,故C选;
D.酸碱中和为放热反应,故D不选.
故选C.
点评 本题考查了反应热与焓变的应用,题目难度不大,明确反应物、生成物总能量与吸热反应、放热反应之间的关系为解答关键,注意掌握常见的吸热反应、放热反应,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该溶液一定有CO32- | |
| B. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 | |
| C. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| D. | 制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
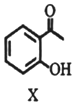 →
→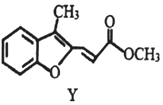 下列说法不正确的是( )
下列说法不正确的是( )| A. | 物质X的分子式为C8H8O2 | |
| B. | 物质X中所有碳原子可能在同一平面内 | |
| C. | 物质Y的1H核磁共振谱图中有8组特征峰 | |
| D. | 1molY最多可与6mol氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 装置 | 步骤 | 现象 |
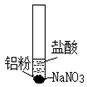 | ⅰ.取少量铝粉于试管,并加入盐酸 | 初始未见明显现象,一段时间后,冒出无色气泡. |
| ⅱ.在试管加入硝酸钠固体 | 继续冒出气泡,液面上方呈浅棕色,试管逐渐变热至沸腾. | |
| ⅲ.用湿润KI-淀粉试纸靠近试管口 | KI-淀粉试纸变蓝色. |
| 装置 | 步骤 | 现象 |
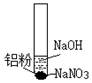 | ⅰ.取少量铝粉于试管,并加入氢氧化钠溶液 | 初始未见明显现象,一段时间后,冒无色气泡. |
| ⅱ.向试管中加入硝酸钠固体 | 继续冒出无色气泡,并有刺激性气味产生 | |
| ⅲ.用湿润红色石蕊试纸靠近试管口 | 试纸变蓝 | |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,Q3Y2与水可剧烈反应,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑
,Q3Y2与水可剧烈反应,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com