
| A. | 使用分液漏斗和容量瓶时,首先要查漏 | |
| B. | 蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,以防止液体暴沸 | |
| C. | 向试管中加液体时,胶头滴管紧贴试管内壁 | |
| D. | 用蒸发皿进行加热蒸发时,一定要垫石棉网 |
分析 A.具有塞子或活塞的仪器使用时要检验是否漏液;
B.加入几粒沸石或碎瓷片,可防止液体剧烈沸腾;
C.胶头滴管应悬空正放;
D.蒸发皿可直接加热.
解答 解:A.具有塞子或活塞的仪器使用时要检验是否漏液,则使用分液漏斗和容量瓶时,首先要查漏,故A正确;
B.加入几粒沸石或碎瓷片,可防止液体剧烈沸腾,则蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,故B正确;
C.向试管中加液体时,不能使胶头滴管紧贴试管内壁,胶头滴管应悬空正放,故C错误;
D.蒸发皿可直接加热,蒸发时不需要垫石棉网,故D错误;
故选CD.
点评 本题考查混合物的分离提纯,为高频考点,把握混合物分离方法实验及仪器的实验为解答的关键,侧重分析与应用能力的考查,注意实验基本操作,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Al3+、SCN-、Cl- | B. | Na+、Ca2+、HCO3-、Cl- | ||
| C. | Fe3+、Na+、S2-、Cl- | D. | K+、H+、Cl-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硬脂酸与软脂酸(C15H31COOH) | B. | HCHO与CH3COOH | ||
| C. | CH2=CHCOOH与CH3CH2CH2COOH | D. | 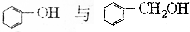 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应鉴别Fe(OH)3胶体和淀粉溶液 | |
| B. | 用渗析的方法除去淀粉胶体含有少量NaCl | |
| C. | 用溶解、过滤、洗涤固体的方法提纯含有少量BaSO4的Na2CO3 | |
| D. | 用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
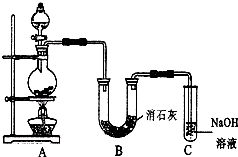 某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应).
某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com