
【题目】中学化学学习过的一些气体可以用如图装置分别制取、干燥和收集,烧杯中的NaOH溶液用于吸收尾气。根据要求回答以下问题。

(1)请分析能用该装置制取、干燥、收集和吸收的气体对反应物、反应条件及气体性质必须符合的要求:
①对反应物的要求:____________;
②对反应条件的要求:___________;
③对生成气体性质的要求:___________。
(2)实验室用高锰酸钾和浓盐酸在如图装置中制取氯气。请回答:
①B中盛放的药品名称是_____;
②C中的现象是________;若C中出现______的现象时,说明反应中没有氯气生成。
③NaOH溶液的作用是_______,反应的化学方程式为___。
【答案】固体或液体与液体反应 不需要加热 生成的气体能被浓硫酸干燥(不具有还原性和碱性)、密度比空气大、能(且需要)用氢氧化钠溶液吸收 浓盐酸 石蕊溶液先变红后褪色 石蕊溶液只变红不褪色 吸收氯气,防止污染空气 Cl2+2NaOH=NaClO+NaCl+H2O
【解析】
(1)由实验装置图可知,制取气体的反应为固(液)、固不加热的反应,气体的密度比空气大,无还原性和碱性,能与氢氧化钠溶液反应;
(2)由实验装置图可知,A中高锰酸钾和浓盐酸反应制备氯气,反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O,洗气瓶中浓硫酸用于干燥氯气,用向上排空气法收集氯气,C中石蕊溶液中通入氯气,溶液先变红后褪色,氢氧化钠溶液用于吸收氯气,防止污染环境。
(1)①由实验装置图可知,图中气体发生装置属于“固(液)+液![]() 气”型,要求反应物的状态为固态和液态,故答案为:固体或液体与液体反应;
气”型,要求反应物的状态为固态和液态,故答案为:固体或液体与液体反应;
②由实验装置图可知,图中气体发生装置属于“固(液)+液![]() 气”型,要求反应条件不加热,故答案为:不需要加热;
气”型,要求反应条件不加热,故答案为:不需要加热;
③由实验装置图可知,实验中采用浓硫酸干燥生成的气体,说明生成的气体无还原性和碱性;采用向上排空气法收集生成的气体,说明生成的气体密度比空气大,且不与空气发生反应;采用NaOH溶液处理尾气,说明生成的气体能被NaOH溶液吸收,故答案为:生成的气体能被浓硫酸干燥(不具有还原性和碱性)、密度比空气大、能(且需要)用氢氧化钠溶液吸收;
(2)①由实验装置图可知,A中高锰酸钾和浓盐酸反应反应制备氯气,分液漏斗B中盛放的是浓盐酸,故答案为:浓盐酸;
②C中盛放的是石蕊试液,氯气与水反应生成盐酸和次氯酸,能使石蕊溶液先变红后褪色;若无氯气生成,挥发出的氯化氢使石蕊溶液只变红但不褪色,故答案为:石蕊溶液先变红后褪色;石蕊溶液只变红不褪色;
③氯气有毒会污染环境,氯气能与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,则NaOH溶液的作用是吸收尾气氯气,防止污染空气,反应的化学方程式为Cl2+2NaOH=NaClO+NaCl+H2O,故答案为:吸收氯气,防止污染空气;Cl2+2NaOH=NaClO+NaCl+H2O。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙、丙分别表示在不同条件下,可逆反应A(g)+B(g)![]() xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
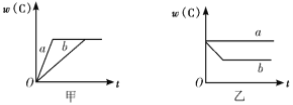

(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则____曲线代表无催化剂时的情况。
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则_______曲线表示恒温恒容的情况,在该情况下混合气体中w(C)_________(填“变大”“变小”或“不变”)。
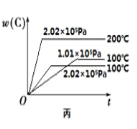
(3)根据丙可以判断该可逆反应的正反应是_____(填“放热”或“吸热”)反应,x的值为________(填范围)。
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是_________________ (填序号)。
①w(C) ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业以浓缩海水为原料提取溴的部分过程如下:
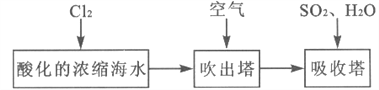
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
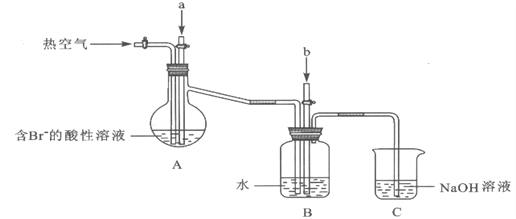
(1)实验开始时,A装置中不通热空气,先通入a气体的目的是(用离子方程式表示)_________。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是_________。
(3)反应过程中,B装置中Br2与SO2反应的化学方程式____________________。
(4)C装置的作用是___________________。
(5)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用____________________方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是________。
(6)某同学提出证明反应后B装置的溶液中含有溴离子的实验方案是:取出少量溶液,先加入过量新制氯水,再加入KI淀粉溶液,观察溶液是否变蓝色。该方案是否合理并简述理由: _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某元素的价类二维图,其中A为正盐,X是一种强碱,通常条件下Z是无色液体,E的相对分子质量比D大16,各物质的转化关系如图所示。下列说法错误的是

A. A作肥料时不适合与草木灰混合施用
B. 同主族元素的氢化物中B的沸点最低
C. C一般用排水法收集
D. D→E的反应可用于检验D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-),温度为T℃时,向20.00mL 0.01mol·L-1氨水中滴入0.10mol·L-1的盐酸(不考虑溶质挥发),溶液的pH和pOH与加入盐酸体积关系如图所示。下列说法正确的是

A. 曲线PJN表示溶液中pH的变化
B. 若M点水的电离程度与Q点相等,则Q点一定符合c(Cl-)>c(NH4+)+c(NH3·H2O)
C. M、P两点的数值之和a+b=14
D. pH与pOH交叉点J对应的V(盐酸)=20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学常见物质且均含有同一种元素,它们之间的部分转化关系如右图所示(反应条件及其他物质已经略去):![]() 。
。
(1)若A为淡黄色固体单质,且D为强酸
①B物质通常用________________(填试剂名称)来检验。
②从组成物质的元素化合价变化角度预测B可能具有的性质_______________ ,并用相应的化学方程式表示你预测的性质_________________________________________。
③一定条件下D转化为B有多种途径,写出其中一种D→B转化的化学方程式
______________________________________________________。
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,D的稀溶液能使湿润的蓝色石蕊试纸变红。
①写出实验室制取A的化学方程式______________________________________。
②B、C都是大气污染物,它们对环境造成的危害表现在_______。
A 引起酸雨 B 引起温室效应 C形成光化学烟雾 D引起水体富营养化
③写出C→D转化的离子方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硝酸锶[Sr(NO3)2]可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:

已知:①“滤液1”的主要溶质是Ca(NO3)2;“滤渣1”的成分为Ba(NO3)2、Sr(NO3)2;“滤渣2”的主要成分为 BaCrO4(杂质不与硝酸反应)。②铬酸(H2CrO4)为弱酸。
(1)“酸浸”不能采用高温的原因是_________________________________。
(2)相对于水洗,用浓HNO3洗涤的优点是_________________________________。
(3)“滤液2”中过量的H2CrO4被N2H4还原为Cr3+,同时放出无污染的气体,写出反应的离子方程式_______________________________________________________。
(4)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=1.0×10-32,当c(Cr3+)降至1.0×10-5mol/L,认为Cr3+已经完全沉淀。现将还原后溶液的pH值调至4,此时Cr3+是否沉淀完全?______________________(列式计算)。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=1.0×10-32,当c(Cr3+)降至1.0×10-5mol/L,认为Cr3+已经完全沉淀。现将还原后溶液的pH值调至4,此时Cr3+是否沉淀完全?______________________(列式计算)。
(5)已知Cr(OH)3类似Al(OH)3,还原后溶液的pH不能大于8的原因是:___________。(结合离子方程式说明理由)。
(6)为了测定“滤渣2”中 BaCrO4的含量,进行以下实验:

①判断Ba2+完全沉淀的方法:____________________________________________。
②“滤渣2”中BaCO4的质量分数为______________________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,可用于水果催熟。A可发生如图所示的一系列 化学反应。
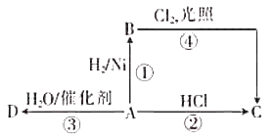
回答下列问题:
(1)C的结构简式为_______________
(2)写出反应③的化学方程式:___________________,该反应是_____________(填反应类型)。
(3)E的相对分子质量是A的两倍,则与A互为同系物的E有________种,写出其中一种的结构简式:_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a%的某物质的水溶液加热蒸发掉mg水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为VL,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( ) mol·L-1。
A.![]() MVB.
MVB.![]() MVC.
MVC.![]() MVD.
MVD.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com