
| 化学键 | N-H | N-N | N≡N | O-H |
| 键能(kJ.mol-1) | 390 | 190 | 946 | 460 |

| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
分析 (1)反应热=反应物总键能-生成物总键能;
(2)①升高温度,反应速率加快,到达平衡时间缩短,平衡向正反应方向移动,NO的产率增大;
②若开始向容器中加入1 mol/L的NO2,发生反应:2NO2(g)?2NO(g)+O2(g),二氧化氮与NO的物质的量之比为1:1,则反应过程中NO的产率与NO的浓度相等,故平衡时NO浓度为0.6mol/L,利用三段式计算平衡时各组分浓度,代入K=$\frac{{c}^{2}(NO)×c({O}_{2})}{{c}^{2}(N{O}_{2})}$计算平衡常数,再计算此时的浓度商Qc,与平衡常数相比判断反应进行方向,进而确定v(正)、v(逆)相对大小;
(3)①X、Y的起始浓度分别为0.2mol/L、0.6mol/L,前10min内,X浓度增大了0.4mol/L、Y的浓度减小0.2mol/L,由于NO2、N2O4与按物质的量2:1反应,则X为NO2、Y为N2O4;
平衡常数K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$,代入物质的浓度计算;
②根据v=$\frac{△c}{△t}$计算v(NO2);20min时,Y(N2O4)的浓度不变,X(NO2)的浓度增大,改变的条件应是增大NO2的浓度,等效为增大压强,平衡向生成N2O4的向逆反应进行,减少2molNO2的同时混合气体总物质的量减小1mol,则混合气体中NO2的百分含量减小.
解答 解:(1)设1mol N2O4(1)完全分解成相应的原子时需要吸收的能量QKJ,则:
190kJ/mol×2+390kJ/mol×8+QkJ/mol-946kJ/mol×3-460kJ/mol×8=-1225 kJ/mol,
解得Q=1793,
故答案为:1793kJ;
(2)①升高温度,反应速率加快,到达平衡时间缩短,平衡向正反应方向移动,NO的产率增大,反应在820℃时进行,NO的产率随时间的变化曲线为: ,
,
故答案为: ;
;
②若开始向容器中加入1 mol/L的NO2,发生反应:2NO2(g)?2NO(g)+O2(g),二氧化氮与NO的物质的量之比为1:1,则反应过程中NO的产率与NO的浓度相等,故平衡时NO浓度为0.6mol/L,则:
2NO2(g)?2NO(g)+O2(g)
开始(mol/L):1 0 0
转化(mol/L):0.6 0.6 0.4
平衡(mol/L):0.4 0.6 0.4
则平衡常数K=$\frac{{c}^{2}(NO)×c({O}_{2})}{{c}^{2}(N{O}_{2})}$=$\frac{0.{6}^{2}×0.4}{0.{4}^{2}}$=0.9,此时的浓度商Qc=$\frac{{1}^{2}×0.2}{0.{5}^{2}}$=0.8<K=0.9,故反应向正反应进行,则v(正)>v(逆),
故答案为:>;
(3)①X、Y的起始浓度分别为0.2mol/L、0.6mol/L,10min时到达平衡,X浓度增大了0.4mol/L、Y的浓度减小0.2mol/L,由于NO2、N2O4与按物质的量2:1反应,则X为NO2、Y为N2O4;
平衡常数K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$=$\frac{0.{6}^{2}}{0.4}$=0.9,
故答案为:0.9;
②v(NO2)=$\frac{0.6mol/L-0.2mol/L}{10min}$=0.04mol/(L.min);20min时,Y(N2O4)的浓度不变,X(NO2)的浓度增大,改变的条件应是增大NO2的浓度,等效为增大压强,平衡向生成N2O4的向逆反应进行,减少2molNO2的同时混合气体总物质的量减小1mol,则混合气体中NO2的百分含量减小,
故答案为:0.04mol/(L.min);增大NO2的浓度;b.
点评 本题考查化学平衡有关计算、化学平衡影响移动、反应热计算等,为高频考点和常见题型,是对学生综合能力的考查,难度中等.


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:实验题
 实验室制备溴苯可用如图所示装置.填空:
实验室制备溴苯可用如图所示装置.填空: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
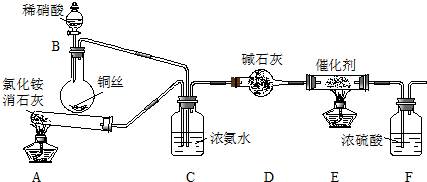
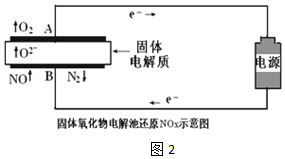
| 实验序号 | B极气体 | 电路中通过电子 | 消耗总电能 | 生成N2 |
| 实验1 | NO | 1mol | a KJ | 0.25mol |
| 实验2 | NO和空气 (不考虑NO2) | 1mol | a KJ | 0.09mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
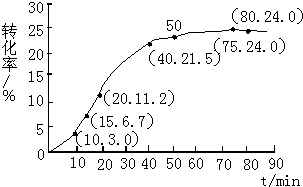 甲酸甲酯水解反应方程式为:
甲酸甲酯水解反应方程式为:| 组分 | HCOOCH3 | H2O | HCOOH | CH3OH |
| 物质的量/mol | 1.00 | 1.99 | 0.01 | 0.52 |
| 反应时间范围/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均反应速率/(10-3mol•min-1) | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 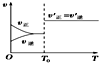 反应H2(g)+I2(g)?2HI(g)达到平衡后,升高温度时反应速率随时间的变化 | |
| B. | 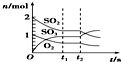 反应2SO2(g)+O2(g)?2SO3(g)达到平衡后,缩小容器容积时各成分的物质的量随时间的变化 | |
| C. |  反应N2(g)+3H2(g)?2NH3(g)在恒温条件下,反应速率与压强的关系 | |
| D. |  反应CO2(g)+H2(g)?CO(g)+H2O(g)△H>0水蒸气含量随时间的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
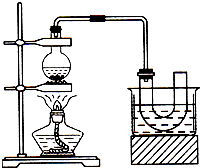 实验室制备溴乙烷(C2H5Br)的装置和步骤如图(已知溴乙烷的沸点38.4℃):
实验室制备溴乙烷(C2H5Br)的装置和步骤如图(已知溴乙烷的沸点38.4℃):查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图为实验室制备乙烯的装置图,请回答:
如图为实验室制备乙烯的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
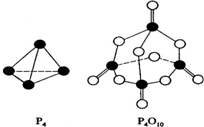 (1)CH3-CH3(g)→CH2=CH2(g)+H2(g);有关化学键的键能如下.
(1)CH3-CH3(g)→CH2=CH2(g)+H2(g);有关化学键的键能如下.| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
| 化学键 | P-P | P-O | P=O | O-O | O=O |
| 键能(kJ/mol) | a | b | c | d | e |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com