
(15分)氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)氢气作为能源最大的优点是燃烧产物是水,无污染。请你再列举一条氢气作为能源的优点:_____________________________________________。
(2)LiAlH4是一种重要的储氢载体,能与水反应得到LiAlO2和氢气,该反应消耗1mol LiAlH4时转移的电子数目为_______________________________________。
(3)氮化锂(Li3N)是非常有前途的储氢材料,其在氢气中加热时可得到氨基锂(LiNH2),其反应的化学方程式为;Li3N+2H2 LiNH2+2LiH,氧化产物为___________(填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的___________%(精确到0.1)。
LiNH2+2LiH,氧化产物为___________(填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的___________%(精确到0.1)。
(4)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:

在某温度下,向恒容密闭容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=__________。
(5)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。

①导线中电子移动方向为__________。(用A、D表示)
②生成目标产物的电极反应式为_______________________________。
③该储氢装置的电流效率η=_________________。
(η= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年黑龙江省高三下学期第一次模考化学试卷(解析版) 题型:填空题
(15分)常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害。某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源

(1)填充物用60 ℃温水溶解,目的是 。
(2)操作A的名称为 。
(3)铜帽溶解时加入H2O2的目的是 (用化学方程式表示)。
铜帽溶解完全后,可采用_____________方法除去溶液中过量的H2O2。
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为 。
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止。主要反应为 2MnO(OH)+MnO2+2H2C2O4+3H2SO4=2MnSO4+4CO2↑+6H2O。
①当1 mol MnO2参加反应时,共有 mol电子发生转移。
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出该反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市门头沟区高三3月综合练习理综化学试卷(解析版) 题型:选择题
下列实验操作能达到预期实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验Fe2(SO4)3溶液中是否含有FeSO4 | 取少量溶液于试管, 加入几滴0.1 mol/L KMnO4溶液 |
B | 证明Al(OH)3是两性氢氧化物 | 取Al(OH)3于试管A、B,分别滴加氨水与盐酸 |
C | 使蛋白质能变性 | 向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,产生沉淀 |
D | 除去Na2CO3中的NaCl | 溶解,加入AgNO3溶液至不再产生沉淀,静置,过滤 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省台州市高三3月调研考试理综化学试卷(解析版) 题型:填空题
(18分)
Ⅰ.浓硝酸与浓盐酸混合过程中会产生少量的气体单质X、化合物M和无色液体,化合物M中所有原子均达到8电子的稳定结构。2molM加热分解生成lmol X和2mol无色气体Y,Y遇到空气呈现红棕色。
(1)镁与气体X反应产物的电子式为 ________。
(2)浓硝酸和浓盐酸反应的化学方程式为 ________。
(3)化合物M水解生成两种酸,为非氧化还原反应,该反应的化学方程式为________。
Ⅱ.石油铁储罐久置未清洗易引发火灾,经分析研究,事故由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1:3反应生成的黑色物质丙自燃引起。某研究小组将一定量的丙粉末投人足量的浓盐酸中发生反应,得到4.8g淡黄色沉淀和气体乙,乙在标准状况下的密度为1.5179g/L,过滤后向滤液(假设乙全部逸出)中加人足量的NaOH溶液, 先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24g,已知气体乙可溶于水。请回答下列问题:
(1)甲的化学式为________。
(2)写出丙中非金属元素的离子结构示意图________。
(3)丙在盐酸中反应的化学方程式:________。(离子方程式表示)
(4)请设计合理的实验方案验证不同温度对丙与盐酸反应速率的影响
(5)为消除火灾隐患,下列措施可行的是 ________。
A.石油入罐前脱硫
B.定期用酸清洗罐体
C.罐体内壁涂刷油漆
D.罐体中充入氮气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省台州市高三3月调研考试理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.在粗盐提纯中,当加热到蒸发皿中有较多固体析出,残留少量液体时,停止加热, 用余热将液体蒸干
B.当振荡分液漏斗中的混合溶液时,须用一只手压住分液漏斗的玻璃塞,另一只手握住旋塞,将分液漏斗倒转过来,用力振荡
C.从加碘盐中获取碘单质的操作步骤为:溶解—萃取—分液—蒸馏
D.实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省洛阳市高三第二次统一考试理综化学试卷(解析版) 题型:选择题
常温下,下列各组微粒在指定溶液中一定能大量共存的是
A.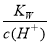 =0.1 mol/L的溶液:K+、Na+、SiO32-、NO3-
=0.1 mol/L的溶液:K+、Na+、SiO32-、NO3-
B.0.1 mol/L AgNO3溶液:H+、K+、SO42-、I-
C.加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-
D.甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省韶关市高三调研考试理综化学试卷(解析版) 题型:填空题
(17分)天然气含有硫化氢气体,回收并综合利用硫化氢有重要的经济价值和环境保护意义。如硫化氢可经过一系列反应制得硫酸:

(1)物质发生不完全燃烧时的反应热难以通过实验测得。已知硫化氢气体的燃烧热是586 kJ/mol,固体硫单质的燃烧热是297 kJ·mol-1。写出硫化氢气体不完全燃烧生成固体硫单质的热化学方程式 。
(2)工业生产中硫化氢尾气可用NaOH溶液吸收。
①吸收尾气后得到的Na2S溶液显 性(填“酸”、“碱”、“中”);
②下列与H2S、NaHS和Na2S相关的离子方程式正确的是(填字母序号)_________。
A.H2S+OH—=HS—+H2O B.HS—+H2O=H2S+OH—
C.HS—+H2O S2—+H3O+ D.S2—+H2O
S2—+H3O+ D.S2—+H2O H2S+2OH—
H2S+2OH—
(3)在一定温度下,某容器中发生2H2S(g) 2H2(g)+S2(g)的反应,测得相应时间时部分物质的浓度(mol·L-1)如下表,根据表中数据回答问题:
2H2(g)+S2(g)的反应,测得相应时间时部分物质的浓度(mol·L-1)如下表,根据表中数据回答问题:
物质 | 0 min | 20 min | 60 min | 90 min | 120 min |
H2S | 0.006 | 0.005 | |||
H2 | 0 | 0.002 | 0.004 | ||
S2 | 0 | 0.002 | 0.0025 |
①判断90 min时反应速率v(正)______v(逆)(填“>”、“=”或“<”);
②求该温度下反应的化学平衡常数(不必写出计算过程)K=______ ___。
(4)以硫化氢为原料,使用质子固体电解质(能传导H+)构成燃料电池,硫化氢放电后生成硫蒸气(化学式S2),该燃料电池的负极反应式为_________ ____。
(5)硫酸是强酸,在图中画出硫酸溶液和氢氧化钠溶液反应过程的能量变化示意图。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一4月月考理科化学试卷(解析版) 题型:选择题
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
A.原子半径 A>B>D>C B.原子序数 d>c>d>a
C.离子半径 C>D>B>A D.单质的还原性 A>B>D>C
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二4月月考化学试卷(解析版) 题型:选择题
科学家最近在-100 ℃的低温下合成了一种键线式为 的烃X,根据分析,下列说法中不正确的是
的烃X,根据分析,下列说法中不正确的是
A.X的分子式为C5H4
B.分子中氢原子的化学环境只有一种
C.1 mol X在一定条件下可与2 mol氢气发生反应
D.X不能使高锰酸钾酸性溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com