
| A. | 将SO2通入BaCl2溶液中至饱和,无沉淀产生,再通入过量NH3,产生沉淀 | |
| B. | 二氧化硫可广泛用于食品的增白 | |
| C. | 用AlCl3溶液制取Al(OH)3,沉淀剂选用氨水比选用NaOH溶液好 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,反应速率加快 |
分析 A.亚硫酸酸性弱于盐酸,二氧化硫能够与氨水反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡沉淀;
B.二氧化硫有毒;
C.氢氧化铝能够溶于强碱;
D.锌和铜在酸性条件下形成原电池反应,反应速率较大.
解答 解:A.亚硫酸酸性弱于盐酸,所以将SO2通入BaCl2溶液中至饱和,无沉淀产生,二氧化硫能够与氨水反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡沉淀,故A正确;
B.二氧化硫有毒不能用于食品漂白,故B错误;
C.一水合氨为弱碱,氢氧化钠为强碱,氢氧化铝不溶于一水合氨溶于氢氧化钠,故C正确;
D.加入少量CuSO4固体,置换出铜,锌和铜在酸性条件下形成原电池反应,反应速率较大,故D正确;
故选:B.
点评 本题考查了元素化合物知识,题目难度中等,熟悉二氧化硫、氢氧化铝的性质是解题关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有SO2、NO、O2 | B. | 肯定没有C12、O2和NO2 | ||
| C. | 可能有Cl2和O2 | D. | 肯定只有NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、OH-、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
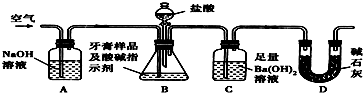
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
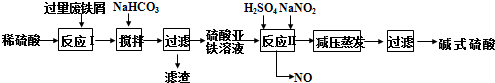
 [Fe2(OH)4]2++2H+.
[Fe2(OH)4]2++2H+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质氧化性的强弱 | |
| B. | 最高价氧化物对应的水化物酸性的强弱 | |
| C. | 单质沸点的高低 | |
| D. | 单质与氢气化合的难易 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H=-akJ•mol-1,则中和热为a/2kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l);△H1=-akJ•mol-1,则氢气燃烧热为akJ•mol-1 | |
| C. | 反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 | |
| D. | N2(g)+3H2(g)?2NH3(g);△H=-akJ•mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 图是2008年北京奥运会的“祥云”火炬,与悉尼奥运火炬所用主要燃料(丁烷)不同,“祥云”火炬所用燃料为丙烷.丙烷和丁烷的沸点如下表:
图是2008年北京奥运会的“祥云”火炬,与悉尼奥运火炬所用主要燃料(丁烷)不同,“祥云”火炬所用燃料为丙烷.丙烷和丁烷的沸点如下表:| 丙烷 | 丁烷 | |
| 沸点/℃ | -42.6 | -0.5 |
| A. | 丙烷燃烧生成的产物无害,是环保型燃料 | |
| B. | 丙烷的沸点比丁烷低,是因为分子间作用力比丁烷弱 | |
| C. | 丙烷在低温时保持的压力比丁烷大 | |
| D. | 丙烷和丁烷都不存在同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com