
| 元素编号 | 元素性质或原子结构 |
| X | 第三周期元素的简单离子中半径最小 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 原子核外电子数和周期序数相等 |

 .
. .
.分析 X是第三周期元素的简单离子中半径最小,则X为Al,Y最简单氢化物丙的水溶液呈碱性,则Y为N元素,丙为NH3,Z原子核外电子数和周期序数相等,则Z为H元素.A、B、D三种单质分别由X、Y、Z元素组成,则A为Al、B为N2、D为H2,丁是一种高能燃料,其组成元素与丙相同,且含有18mol电子,则丁为N2H4;Al与氮气反应生成甲为AlN,AlN水解得到氨气与氢氧化铝,故戊为Al(OH)3,乙为Al2O3,据此解答.
解答 解:X是第三周期元素的简单离子中半径最小,则X为Al,Y最简单氢化物丙的水溶液呈碱性,则Y为N元素,丙为NH3,Z原子核外电子数和周期序数相等,则Z为H元素.A、B、D三种单质分别由X、Y、Z元素组成,则A为Al、B为N2、D为H2,丁是一种高能燃料,其组成元素与丙相同,且含有18mol电子,则丁为N2H4;Al与氮气反应生成甲为AlN,AlN水解得到氨气与氢氧化铝,故戊为Al(OH)3,乙为Al2O3.
(1)元素X为Al,在周期表中的位置是:第三周期第ⅢA族,其简单离子的结构示意图为 ,
,
故答案为:第三周期第ⅢA族; ;
;
(2)单质B为N2,电子式为 ,故答案为:
,故答案为: ;
;
(3)丙为NH3,N原子与H原子之间形成极性共价键,故选:b;
(4)反应②为氨气与NaClO的反应,0.5molNaClO参加反应时,转移1mol电子,则Cl元素由+1价降低为-1价,该反应生成NaCl,同时生成N2H4和水,则该反应为2NH3+NaClO═N2H4+NaCl+H2O,
故答案为:2NH3+NaClO═N2H4+NaCl+H2O;
(5)一定条件下,Al与TiO2、C(石墨)反应只生成Al2O3和碳化钛(TiC),该化学方程式为:4Al+3TiO2+3C═2Al2O3+3TiC,
故答案为:4Al+3TiO2+3C═2Al2O3+3TiC.
点评 本题考查无机物的推断,侧重于学生的分析推理能力的考查,需要学生熟练掌握元素化合物性质,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 与
与 互为同分异构体
互为同分异构体 与
与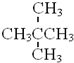 属于同系物
属于同系物 与
与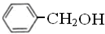 既不是同系物也不是同分异构体.
既不是同系物也不是同分异构体.| A. | ①⑤ | B. | ①④ | C. | ①③⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 纯铁的腐蚀属于电化学腐蚀 | |
| B. | 钢铁吸氧腐蚀时,负极的电极反应式为Fe-3e-═Fe3﹢ | |
| C. | 海轮在浸水部位镶一些铜锭可起到抗腐蚀作用 | |
| D. | 在图示氧浓差腐蚀中,M极处发生的电极反应为O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与P4的分子结构都是正四面体形,因此在6.02×1023个CH4分子或P4分子中都含有4×6.02×1023个共价键 | |
| B. | 在含6.02×1023个硅原子的二氧化硅晶体中含有4×6.02×1023个Si-O键 | |
| C. | 5.6 g Fe与含0.2 mol HNO3的溶液充分反应,至少失去0.2×6.02×1023个电子 | |
| D. | 6.02×1023个Fe3+完全水解可以得到6.02×1023个氢氧化铁胶体粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时.将电能转化成化学能 | |
| B. | 充电时,阳极反应为Li++e-═Li | |
| C. | 正极的电极反应式为FeS2+2e-+2Li+═Li2FeS2 | |
| D. | 每转移0.1mol电子,正极材料消耗12.0g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com