
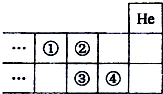
| A、①的气态氢化物比②的稳定 |
| B、②的最高价含氧酸的酸性比③强 |
| C、③的非金属性比④强 |
| D、④的原子半径比③小 |


科目:高中化学 来源: 题型:
| A、正极 Zn 负极 Cu 电解质溶液 CuCl2 |
| B、正极Cu 负极Zn 电解质溶液 CuCl2 |
| C、正极Zn 负极Cu 电解质溶液 ZnCl2 |
| D、正极Cu 负极Zn 电解质溶液 ZnCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 把MgSO4溶液滴入Ba(OH)2溶液 | Mg2++2OH-═Mg(OH)2↓ | 正确 |
| B | 向小苏打溶液中加足量氢氧化钠溶液 | HCO3-+OH-═CO2↑+H2O | 正确 |
| C | 向FeCl2溶液中通入氯气 | 2Fe2++Cl2═2Fe3++2Cl- | 不正确 |
| D | 氧化钙与稀盐酸反应 | CaO+2H+═Ca2++H2O | 正确 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
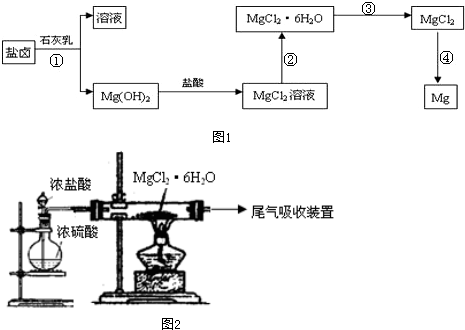
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯可发生加成反应 |
| B、石油干馏可得到汽油、煤油等 |
| C、淀粉、蛋白质完全水解的产物互为同分异构体 |
| D、从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com