
���� I����1��H2O2+2KI+H2SO4=I2+K2SO4+2H2O��O��-1�۽��͵�-2�ۣ�I��-1�����ߵ�0�ۣ�ת�Ƶ�����Ϊ2��
��2����Ӧ�����У�I2���뷴Ӧ�����������ɵ�����I2���ӿ��������ķֽ⣬I2��������ã�
II���ӵ���غ�ĽǶȷ���������ƽ��Ӧ�����ӷ���ʽ��3Fe2++2S2O32-+O2+4OH-�TFe3O4+S4O62-+2H2O����Ӧ��3Fe2+��Fe3O4����3molFe2+�μӷ�Ӧʱ����2molFe2+���ϼ����ߣ���Ӧ��Fe��SԪ�صĻ��ϼ����ߣ���Fe2+��S2O32-�ǻ�ԭ����OԪ�صĻ��ϼ۽��ͣ���O2Ϊ��������
��� �⣺��1��H2O2+2KI+H2SO4=I2+K2SO4+2H2O��O��-1�۽��͵�-2�ۣ�I��-1�����ߵ�0�ۣ�ת�Ƶ�����Ϊ2������˫���ŷ���ʾ����ת��Ϊ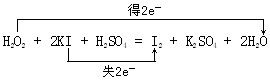 ��
��
�ʴ�Ϊ��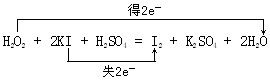 ��
��
��2����Ӧ�����У�I2���뷴Ӧ�����������ɵ�����I2���ӿ��������ķֽ⣬I2��������ã�
�ʴ�Ϊ��������
II����1����Ӧ��FeԪ�ػ��ϼ۲�������Ϊ+3�ۣ�SԪ�ػ��ϼ���+2�����ߵ�+2.5�ۣ���ԭ����Fe2+��S2O32-�����ݻ��ϼ۴�����Ϊ0����S2O32-��S�Ļ��ϼ�Ϊ+2���ʴ�Ϊ��Fe2+��S2O32-��+2��
��2��Fe��SԪ�صĻ��ϼ����ߣ�OԪ�صĻ��ϼ۽��ͣ��ɷ�Ӧ��֪���÷�Ӧת��4e-������ÿ����1mol Fe3O4����OԪ�صĻ��ϼ۱仯��֪��ת�Ƶ���Ϊ1mol��2��[0-��-2��]=4mol��
�ʴ�Ϊ��4��
���� �����ۺϿ���������ԭ��Ӧ�������ڿ���ѧ�������ݷ����������ۺ����û�ѧ֪ʶ����������Ŀ�Ѷ��еȣ�ע�����������ǿ���ıȽϷ�����


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
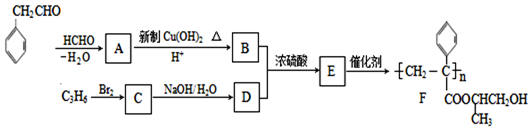
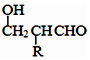 $\stackrel{-H_{2}O}{��}$
$\stackrel{-H_{2}O}{��}$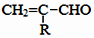
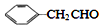 ��Ϊͬϵ���G���ʵ���Է���������
��Ϊͬϵ���G���ʵ���Է���������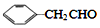 ��14�ģ����������������G��ͬ���칹����9�֣�
��14�ģ����������������G��ͬ���칹����9�֣�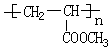 �ĺϳ�·��
�ĺϳ�·��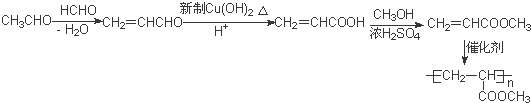 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��O$\stackrel{HCN}{��}$
��O$\stackrel{HCN}{��}$ $\stackrel{H_{2}O/H+}{��}$
$\stackrel{H_{2}O/H+}{��}$
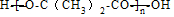 +��n-1��H2O��
+��n-1��H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 A��B��C��D��E��Ϊ�л������A�ǻ�ѧʵ����������л����������ˮ����������ζ��B�IJ����ɺ���һ������ʯ�ͻ�����չ��ˮƽ���й����ʵ�ת����ϵ��ͼ��ʾ��
A��B��C��D��E��Ϊ�л������A�ǻ�ѧʵ����������л����������ˮ����������ζ��B�IJ����ɺ���һ������ʯ�ͻ�����չ��ˮƽ���й����ʵ�ת����ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 46g NO2��N2O4�Ļ�������к��е�ԭ�Ӹ���Ϊ3NA | |
| B�� | 1 mol Na2O2��ˮ��ȫ��Ӧʱת�Ƶ�����Ϊ2NA | |
| C�� | ��״���£�2.24L���麬�еķ�����Ϊ0.1NA | |
| D�� | 1 mol Na2O2�к��е���������Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ�� | ���� | ���� | |
| A | Fe��OH ��3 ����ͨ��� | ���������ɫ���� | Fe��OH��3����� ���� |
| B | ��ͭ�ۼ��� 1.0mol•L-1 ��Fe2��SO4��3��Һ�� | ��Һ�������к�ɫ������� | ����Fe��Cu�� �� |
| C | ������ǯ��ס��ɰֽ ��ϸ��ĥ���������� �ƾ����ϼ��� | �ۻ����Һ̬���������� | ���������۵�� �ϵ� |
| D | ��ʢ������Ũ���ᡢ ϡ�������֧�Թ��� �ֱ����һƬ��С�� ͬ��ͭƬ | Ũ������ͭƬ�ܿ쿪ʼ�ܽ⣬���ų� ����ɫ���壻ϡ�����й�һ��ͭƬ�� ��ų�����ɫ���壬������������� ��ɫ | Ũ����������ǿ ��ϡ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��ˮ�⣺HCO3-+H2O?H3O++CO32- | |
| B�� | ����ĵ��룺CH3COOH�TCH3COO-+H+ | |
| C�� | ̼��Ƶ��ܽ�ƽ�⣺CaCO3��s��?Ca2+��aq��+CO32-��aq�� | |
| D�� | H2��ȼ����Ϊ285.8 kJ/mol�����ʾH2ȼ���ȵ��Ȼ�ѧ����ʽΪ��H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-285.8 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
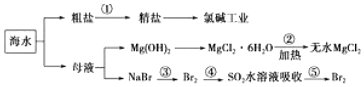
| A�� | �����Ƿ绯���� | |
| B�� | �ڹ��ۢܢ�����Ԫ�ؾ������� | |
| C�� | ��ҵ�ϵ������״̬�µ��Ȼ�þ��ȡþ���� | |
| D�� | �����г�ȥ�����е�SO42-��Ca2+��Mg2+��Fe3+�����ʣ������ҩƷ˳��ΪNa2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com