
【题目】某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( ) 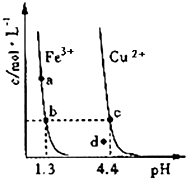
A.该温度下,Ksp[Fe(OH)3]>Ksp[Cu(OH)2]
B.c、d 两点代表的溶液中c(H+) 与c(OH﹣) 乘积不相等
C.Cu(OH)2在c点比在d点代表的溶液中溶解程度小
D.加适量浓NH3H2O可使溶液由a点变到b点
【答案】D
【解析】解:A.由b、c两点对应数据可比较出KSP[Fe(OH)3]与KSP[Cu(OH)2]的大小,KSP[Fe(OH)3]=c(Fe3+)(OH﹣)3=c(Fe3+)(10﹣12.7)3 , KSP[Cu(OH)2]=c(Cu2+)(OH﹣)2=c(Cu2+)(10﹣9.6)2 , 因c(Fe3+)=c(Cu2+),故KSP[Fe(OH)3]<KSP[Cu(OH)2],故A错误;
B.只要温度不发生改变,溶液中c(H+)与c(OH﹣)的乘积(即Kw)就不变.该题中温度条件不变,故c、d两点代表的溶液中c(H+)与c(OH﹣)的乘积相等,故B错误;
C.在C点表示饱和溶液,在d点表示不饱和溶液,所以Cu(OH)2在c点比在d点代表的溶液中溶解程度大,故C错误;
D.向溶液中加入氨水,溶液的pH增大,则铁离子浓度降低,所以可以由a点变到b点,故D正确.
故选D.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】关于如图所示转化关系(X代表卤素),说法不正确的是( ) 
A.2H(g)+2X(g)=2HX(g)△H3<0
B.途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3
C.途径Ⅰ生成HBr放出的热量比生成HCl的少,说明HBr比HCl稳定
D.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃均可由石油加工得到,其球棍模型如图所示。
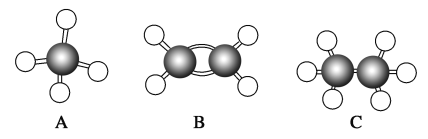
(1)在相同条件下,等体积的以上三种物质完全燃烧时消耗氧气最多的是________(填对应字母,下同);
(2)等质量的以上三种物质完全燃烧时,消耗氧气由多到少的顺序是________;
(3)在120℃、1.01×105 Pa时,有两种气态烃和足量的氧气混合点燃,相同条件下测反应前后气体体积,没有发生变化,这两种气态烃是________;
(4)写出B转化为C的化学方程式:____________________;
(5)除去气体C中混有的少量B可选用的试剂名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子.元素Y的负一价离子的最外层电子数与次外层的相同.回答下列问题:
(1)单质M的晶体类型为 , 晶体中原子间通过作用形成面心立方密堆积,其中M原子的配位数为 .
(2)元素Y基态原子的核外电子排布式为 , 其同周期元素中,第一电离能最大的是(写元素符号).元素Y的含氧酸中,酸性最强的是(写化学式),该酸根离子的立体构型为 .
(3)M与Y形成的一种化合物的立方晶胞如图所示. ①该化合物的化学式为 , 已知晶胞参数a=0.542nm,此晶体的密度为gcm﹣3 . (写出计算式,不要求计算结果.阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是 . 此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为 . 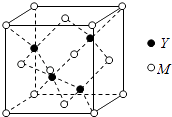
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列萃取与分液结合进行的操作(用CCl4为萃取剂从碘水中萃取碘)中错误的是
A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用左手压住分液漏斗上口部,右手握住活塞部分,把分液漏斗倒转过来振荡
B.静置,分液漏斗中溶液分层,下层呈紫红色,上层几乎无色
C.打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出
D.最后继续打开活塞用另一个烧杯承接上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的是( )
A. 用如图所示装置除去Cl2中含有的少量HCl
用如图所示装置除去Cl2中含有的少量HCl
B.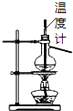 如图所示为石油分馏
如图所示为石油分馏
C.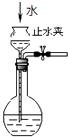 如图所示为检查装置气密性
如图所示为检查装置气密性
D. 如图所示为测定未知盐酸的浓度
如图所示为测定未知盐酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s)═N2(g)+CO2(g)△H=﹣213.5kJ mol﹣1 , 达到平衡时的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | |
T2 | 0.25 |
下列说法不正确的是( )
A.上述信息可推知:T1<T2
B.T1℃时,该反应的平衡常数K= ![]()
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
D.T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是
A.Fe B.葡萄糖 C.MgSO4 D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在200℃时,将a mol H2(g)和b mol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)2HI(g)。
(1)反应刚开始时,由于c(H2)=______,c(I2)=______,而c(HI)=________,所以化学反应速率________最大而________最小(为零)(填“v正”或“v逆”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)________,c(I2)________,而c(HI)________,从而化学反应速率v正________,而v逆________(填“增大”、“减小”或“不变”)。
(3)当反应进行到v正与v逆________时,此可逆反应就达到了最大限度,若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率及体系的总压强(或各组分的分压)都将________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com