
【题目】聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确的是( )
A.KClO3作氧化剂,每生成1mol [Fe(OH)SO4]n消耗![]() mol KClO3
mol KClO3
B.绿矾长时间置于空气中易被氧化
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.聚合硫酸铁与漂白粉都是纯净物
【答案】D
【解析】
A、1mol [Fe(OH)SO4]n中含n mol Fe3+,则每生成1mol [Fe(OH)SO4]n转移电子n mol,而KClO3的还原产物为Cl-,则1mol KClO3被还原,需要转移电子6mol,由于在氧化还原反应中得失电子数目相同,故每生成1mol [Fe(OH)SO4]n消耗![]() mol KClO3,A正确;
mol KClO3,A正确;
B、绿矾(FeSO4·7H2O)晶体中含Fe2+,该物质易被空气氧化,B正确;
C、聚合硫酸铁可在水中水解形成氢氧化铁胶体而净水,C正确;
D、聚合硫酸铁[Fe(OH)SO4]n中的“n”值不能确定,故该物质为混合物;漂白粉是氢氧化钙、氯化钙、次氯酸钙的混合物;D错误;
故选D。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法错误的是
A.标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为9NA
B.56g铁在足量氧气中完全燃烧,转移的电子数小于3NA
C.16g O2和14C2H4的混合物中所含中子数为8NA
D.常温下,1 L 0.5 mol/L CH3COONH4溶液的pH=7,则溶液中CH3COO-与NH4+的数目均为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业中的用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH-===2NO2-+H2O;
②气体液化的温度:NO2为21 ℃,NO为-152 ℃。
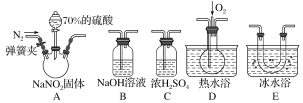
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接)为A、C、________、________、________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是________________________________________________________________________。
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是________________________。
②装置E的作用是_________________________________________________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为___________。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体,发生化学反应生成另外两种气体,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
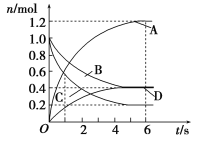
A. 该反应的化学方程式为3B(g)+4D(g)![]() 6A(g)+2C(g)
6A(g)+2C(g)
B. 反应进行到1 s时,v(A)=v(D)
C. 反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D. 反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的F2和ClF混合,在密闭容器中发生反应:F2(g)+ClF(g)![]() ClF3(g) ΔH<0。下列叙述正确的是
ClF3(g) ΔH<0。下列叙述正确的是
A.保持恒容,平衡后再降低温度,平衡常数减小
B.若增加F2的用量,平衡正向移动,则反应物的转化率均增大
C.达到平衡后,若增大容器体积,则正反应速率减小,逆反应速率增大,平衡左移
D.恒温恒容时,当ClF转化40%时,容器内的压强为初始时的0.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。

请回答:
(1)虚线框处宜选择的装置是___(填“甲”或“乙”);实验时应将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净氢气中,观察到的实验现象是___。
(2)硬质玻璃管中铁和水蒸气反应的化学方程式为___(并用单线桥表示电子转移情况)。取硬质玻璃管中适量的固体,用一定浓度的盐酸溶解,滴加KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁,判断结论是否正确并用文字和离子方程式说明理由___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A. Fe + CuSO4 = FeSO4+ Cu
B. AgNO3+ NaCl= AgCl↓ + NaNO3
C. MnO2 + 4 HCl(浓) ![]() MnCl2+ Cl2↑ + 2 H2O
MnCl2+ Cl2↑ + 2 H2O
D. 2KMnO4 ![]() K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+3B2(g)![]() 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1mol A2、3molB2 | 2molAB3 | 2mol AB3 |
反应物的转化率 | a甲 | a乙 | a丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
平衡时AB3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A. v甲=v丙 B. c乙< c丙 C. a甲 +a乙<1 D. K乙≤K丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
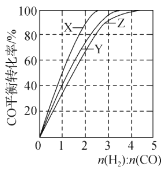
A.下图是在不同温度下三个恒容容器中反应2H2(g)+CO(g)CH3OH(g) △H<0的平衡曲线,曲线X对应的温度相对较高
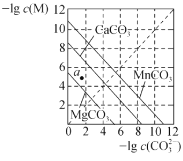
B.下图是一定温度下三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线,a点可表示MgCO3的过饱和溶液,且c(Mg2+)>c(CO32-)
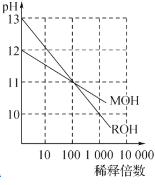
C.下图为MOH和ROH两种一元碱水溶液在常温下分别加水稀释时pH值的变化曲线,可知ROH是强碱
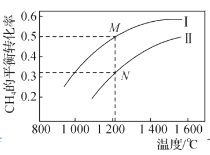
D.下图为两个1L容器中各投入1molCH4和1molCO2所发生反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡曲线,N点化学平衡常数K=1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com