
化学-物质结构与性质:
根据下列五种1-20号元素的电离能数据(单位:kJ/mol),回答下列问题.
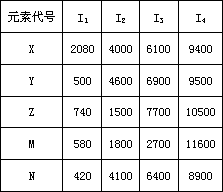
(1)据上表可推断,上述五种元素,处于周期表中同一族的是________(填字母).
A.X和Y B.Z和M C.M和N D.Y和M E.Y和N
(2)电解它们熔融的最高价氧化物,阴极电极反应式正确的是________(填字母).
A.X2++2e-→X
B.Y2++2e-→Y
C.Z3++3e-→Z
D.M3++3e-→M
E.N2++2e-→N
(3)若X元素原子的最外层有2个P电子,则X的氢化物的化学键类型是________,其空间构型是________.
(4)M元素原子的最外层电子排布式是________,Z元素的单质形成的晶体类型是________.
科目:高中化学 来源: 题型:阅读理解
| 元 素 | M | F | |
| 电离能 (kJ?mol-1) |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| N | 2- 2 |
| N | 2- 2 |
| N | 2- 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 【化学--选修物质结构与性质】
【化学--选修物质结构与性质】查看答案和解析>>
科目:高中化学 来源: 题型:
 [化学-选修物质结构与性质]
[化学-选修物质结构与性质]查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com