
| 实验操作 | 预期现象 | 结论 |
| 实验1:在试管A加入少量乙醚,充分振荡,静置 | 乙醚层呈红色 | “猜想一”不成立 |
| 实验2:取萃取后的上层清液滴加2-3滴 K4[Fe(CN)6]溶液 | 若产生蓝色沉淀 | 则“猜想二”成立 |
分析 (1)步骤1KI和FeCl3发生氧化还原反应生成I2、KCl和FeCl2;
(2)Fe(SCN)3在乙醚溶解度较大,显红色;
Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀
解答 解:(1)步骤1:活动(Ⅰ)KI和FeCl3发生氧化还原反应生成I2、KCl和FeCl2,发生反应:2KI+FeCl3=I2+2KCl+FeCl2,其离子反应为2Fe3++2I-=2Fe2++I2,
故答案为:2Fe3++2I-=2Fe2++I2;
(2)由信息一可得:往探究活动III溶液中加入乙醚,Fe(SCN)3在乙醚溶解度较大,充分振荡,乙醚层呈血红色,
由信息信息二可得:取萃取后的上层清液滴加2-3滴K4[Fe(CN)6]溶液,产生蓝色沉淀,
故答案为:
| 实验操作 | 现象 | 结论 |
| 乙醚层呈红色 | “猜想一”不成立 | |
| 取萃取后的上层清液滴加2-3滴 K4[Fe(CN)6]溶液 |
点评 本题主要考查了氧化还原反应、离子方程式的书写、反应的限度的探究,题目难度中等,抓住题干提供的信息是解答问题的关键,注意把握离子的检验方法,侧重于考查学生的分析能力和实验探究能力.


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:多选题
| A. | 平衡常数K增大 | B. | a+b<c+d | C. | X的转化率下降 | D. | Z的体积分数增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浸泡高锰酸钾溶液的硅土来吸收水果或花朵产生的乙烯以达到保鲜效果 | |
| B. | 淀粉、油脂、蛋白质都是天然高分子化合物 | |
| C. | 加热能杀死流感病毒是因为病毒的蛋白质受热变性 | |
| D. | 含硫化石燃料的大量燃烧是酸雨形成的主要原因之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
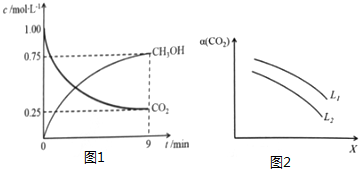 随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点..“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.(1)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点..“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.(1)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com