
在配制物质的量浓度溶液时,下列操作出现的后果是(填:“溶液浓度不准确”、“偏低”、“偏高”、“无影响”):
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体。_____________。
(2)配制氯化钠溶液时,容量瓶中有少量水。______________。
(3)配制好溶液后,容量瓶未塞好,洒出一些溶液。_____________。
(4)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线
科目:高中化学 来源: 题型:阅读理解
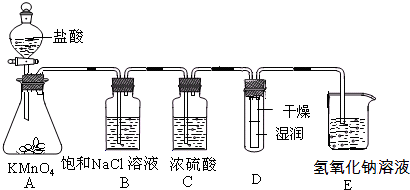
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室现需配制物质的量浓度为1 mol·L-1的NaOH溶液480 mL。
(1)实验过程中用到的玻璃仪器有:烧杯、量筒、胶头滴管、________、________。
(2)要配制此溶液,需要称量NaOH固体的质量为________。
(3)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请解释原因(用化学方程式表示)________________________________。
(4)若将此溶液长期暴露在空气中,最终转化为________,取一定量的该物质溶于水配制成饱和溶液,通入CO2气体后发现溶液变浑浊,写出发生反应的化学方程式
____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)实验室现需配制物质的量浓度为1 mol·L-1的NaOH溶液480 mL。
(1)实验过程中用到的玻璃仪器有:烧杯、量筒、胶头滴管、________、________。
(2)要配制此溶液,需要称量NaOH固体的质量为________。
(3)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请解释原因(用化学方程式表示)________________________________。
(4)若将此溶液长期暴露在空气中,最终转化为________,取一定量的该物质溶于水配制成饱和溶液,通入CO2气体后发现溶液变浑浊,写出发生反应的化学方程式
____________________________________。
查看答案和解析>>
科目:高中化学 来源:鲁必修1综合卷 题型:实验题
(10分)实验室现需配制物质的量浓度为1 mol·L-1的NaOH溶液480 mL。
(1)实验过程中用到的玻璃仪器有:烧杯、量筒、胶头滴管、________、________。
(2)要配制此溶液,需要称量NaOH固体的质量为________。
(3)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请解释原因(用化学方程式表示)________________________________。
(4)若将此溶液长期暴露在空气中,最终转化为________,取一定量的该物质溶于水配制成饱和溶液,通入CO2气体后发现溶液变浑浊,写出发生反应的化学方程式
____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届广东省深圳市高一上学期期中联考化学试卷 题型:选择题
用下列方案配制物质的量浓度为1mol/L的溶液,其中可行的是( )
A.将10gNaOH溶解在少量水中,再加蒸馏水直到溶液体积为250ml
B.用托盘天平称量5.85gNaCl固体,配成100ml溶液
C.将常温常压下11.2LHCl气体溶于水,配成500ml溶液
D.将40gNaOH溶解在1L水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com