
有一种微型电池,其电极分别为Zn和Ag2O,电解质溶液是KOH溶液,试回答下列问题:
(1)原电池是把 能转化成 能的装置.
(2)该电池中Zn极为 极.电极反应式为 .
(3)当金属Zn消耗了16.25g时,转移电子的物质的量为 mol.
考点:
原电池和电解池的工作原理.
分析:
(1)原电池是将化学能转化为电能的装置;
(2)在原电池中,较活泼、失电子的物质作负极;
(3)根据负极电极反应:Zn+2OH﹣═Zn(OH)2+2e﹣来计算电子转移的量.
解答:
解:(1)原电池是将化学能转化为电能的装置,故答案为:化学;电;
(2)在该原电池中,金属锌较活泼且发生失电子反应,电极反应式为Zn﹣2e﹣=Zn2+,故答案为:负;Zn﹣2e﹣=Zn2+;
(3)负极电极反应:Zn+2OH﹣═Zn(OH)2+2e﹣,当金属Zn消耗了16.25g即0.25mol时,转移电子的物质的量为0.5mol,故答案为:0.5.
点评:
本题考查学生原电池的能量转化以及工作原理和电子守恒的计算等知识,属于基础知识的考查,难度不大.


科目:高中化学 来源: 题型:
化学实验中的很多气体是用盐酸来制取,这导致这些制
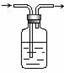
取的气体中往往含有 HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用右图所示装置。如果广口
瓶中盛装的是饱和NaHCO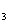 溶液,则可用作下列哪种气体的除杂装置是( )
溶液,则可用作下列哪种气体的除杂装置是( )
A.CO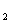 B. Cl
B. Cl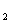 C.H
C.H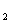 S D.H
S D.H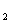
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式
的是 ( )
A.向碳酸氢铵溶液中加入过量的NaOH固体 NH4++OH-= NH3↑+H2O
B.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C.铜片插入硝酸银溶液中 Cu + Ag+ = Cu2+ + Ag
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对阿伏加德罗定律及推论的理解不正确的是( )
A.同温同压下,气体的体积之比等于它们的物质的量之比
B.同温同压下,气体的体积之比等于它们的质量之比
C.同温同压下,相同体积的气体质量比等于它们的相对分子质量之比
D.同温同压下,气体的密度之比等于它们的相对分子质量之比
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能大量共存的是( )
A.Na+、Al3+、NO3-、H+ B.Ba2+、Na+、Cl-、SO42-
C.Mg2+、H+、SO42-、OH- D.H+、Na+、CO32-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com