
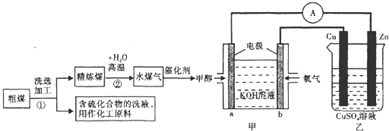
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| C | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | … | 6 |
| 2 | 900 | 6 | 3 | … | 1.5 | 3 |
| 3 | 900 | … | … | … | … | 1 |
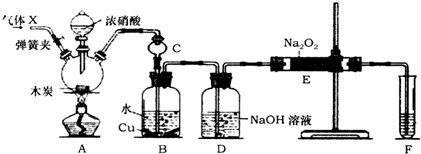
分析 (1)甲池为原电池,负极通入甲醇,发生氧化反应,在碱性条件下生成碳酸根离子和水;
池为原电池,与电源正极相连的铜为阳极,铜失去电子发生氧化反应;锌为阴极,铜离子得到电子反应还原反应,依此进行解答;
(2)根据盖斯定律,由(①-②)÷2得出正确结论;
(3)①根据平衡时各物质的浓度,结合平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积进行计算;
减小压强,平衡向着气体体积增大的方向移动,依此进行判断;
②根据等效平衡进行判断.恒容密闭容器,转到一边,实验2、3的起始投料量相等.
解答 解:(1)甲池为原电池,负极通入甲醇,发生氧化反应,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O;
乙池为原电池,与电源正极相连的铜为阳极,发生氧化反应,电极反应式为:Cu-2e-═Cu2+,锌为阴极,发生还原反应,电极反应式为:Cu2++2e-=Cu,故的电解质溶液的pH不变,
故答案为:不变;CH3OH-6e-+8OH-=CO32-+6H2O;
(2)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O△H=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
由(①-②)÷2得,CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=$\frac{(-1451.6kJ/mol)-(-566kJ/mol)}{2}$=-442.8kJ/mol,
故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H═-442.8kJ/mol;
(3)①实验2中达到平衡时,c(CO)=c(H2)=$\frac{1.5mol}{2L}$=0.75mol/L,c(H2O)=$\frac{3mol-1.5mol}{2L}$=0.75mol/L,
K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$=$\frac{0.75×0.75}{0.75}$=0.75;
实验2中分离出1molH2O(g),则体系压强减小,平衡正向移动,H2O(g)的转化率增大,
故答案为:0.75;增大;
(3)实验3起始时充入的是CO(g)和H2(g),且达平衡时实验2、3中CO的体积分数相同,说明两者为等效平衡,且为恒容密闭容器,故转到一边,实验2、3的起始投料量相等.实验2的起始投料为3molH2O,全部转到右边,相当于3molCO和3molH2,故实验3起始时应加入3molCO和3molH2,故c(H2)=$\frac{3mol}{2L}$=1.5mol/L,
故答案为:1.5mol/L.
点评 本题考查较为综合,涉及原电池和电解池的电极反应式的书写、盖斯定律的应用、平衡常数的计算、及等效平衡等知识,为高考常见题型,侧重于学生的分析能力和实验能力的考查,综合性较强,难度较大.


 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | 油脂是高级脂肪酸和甘油生成的酯 | |
| B. | 米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 银盐 性质 | AgCl | AgBr | Ag2CrO4 |
| 颜色 | 白 | 浅黄 | 砖红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制NaOH标准液时,所用的NaOH固体中含有少量的KOH杂质 | |
| B. | 滴定前对碱式滴定管仰视读数,滴定后又俯视 | |
| C. | 滴定前,碱式滴定管尖嘴部分有气泡,滴定后气泡消失 | |
| D. | 碱式滴定管用蒸馏水洗净后,直接装入标准NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
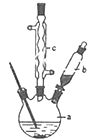 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,下面是它的一种实验室合成路线: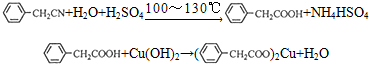
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.80 | 20.01 | 20.00 | 19.99 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
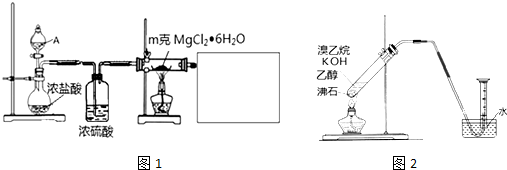
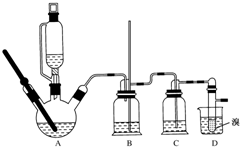 用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
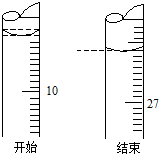 某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com