
| A. | 溶液的pH值:①>③>② | |
| B. | 水电离出的c(OH-):③>①=② | |
| C. | ①和③等体积混合后的溶液:c(CH3COOH)+c(CH3COO-)=0.1mol/L | |
| D. | ②和③等体积混合后的溶液:c(Na+)=c(CH3COOH)+c(CH3COO-) |
分析 A.常温下,相同浓度的这几种溶液的pH大小顺序是:碱>强碱弱酸盐>酸;
B.酸或碱抑制水电离,且酸中氢离子浓度越大或碱中c(OH-)越大其抑制水电离程度越大;含有弱离子的盐促进水电离;
C.①和③等体积混合后,溶液体积增大一倍,溶液中粒子浓度降为原来的一半;
D.②和③等体积混合后的溶液中存在物料守恒,根据物料守恒判断.
解答 解:A.常温下,相同浓度的这几种溶液的pH大小顺序是:碱>强碱弱酸盐>酸,所以这几种溶液的pH大小顺序是②>③>①,故A错误;
B.酸或碱抑制水电离,且酸中氢离子浓度越大或碱中c(OH-)越大其抑制水电离程度越大;含有弱离子的盐促进水电离,①②抑制水电离,且抑制水电离程度②>①,③促进水电离,所以水电离程度大小顺序是③>①>②,故B错误;
C.①和③等体积混合后,溶液体积增大一倍,溶液中粒子浓度降为原来的一半,根据物料守恒得c(CH3COOH)+c(CH3COO-)=0.1mol/L,故C正确;
D.②和③等体积混合后的溶液中存在物料守恒,根据物料守恒得c(Na+)=2[c(CH3COOH)+c(CH3COO-)],故D错误;
故选C.
点评 本题考查离子浓度大小比较、酸碱混合溶液定性判断等知识点,为高频考点,侧重考查学生分析判断能力,明确等体积混合后溶液体积增大一倍是解本题关键,易错选项是C.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:选择题
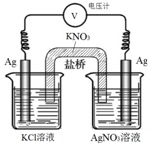 一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 右池中的银电极作负极 | B. | 总反应为Ag++Cl-=AgCl | ||
| C. | 正极反应为Ag-e-=Ag+ | D. | 盐桥中的NO3-向右池方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥ | B. | ①④⑥ | C. | ①④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | 无色溶液中:Cu2+、Al3+、NH4+、Cl- | |
| C. | 由水电离出的c(H+)=1×10-13mol•L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| D. | 0.1mol•L-1FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
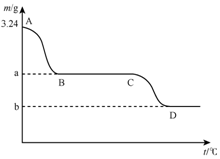 取3.24g碳酸氢钙在高温条件下分解,固体质量变化与温度的关系如图所示,试根据要求回答下列问题:
取3.24g碳酸氢钙在高温条件下分解,固体质量变化与温度的关系如图所示,试根据要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的质量不再改变 | |
| B. | 混合气的密度不再随时间而变化 | |
| C. | 容器内的压强不随时间而变化 | |
| D. | 单位时间内生成2a mol B,同时生成a mol C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HCl>HI | B. | 原子半径:Na>Mg | ||
| C. | 酸性:H2SiO3>H2SO4 | D. | 氧化性:Cl2>S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气的水溶液可以导电,说明氯气是电解质 | |
| B. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| C. | 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 | |
| D. | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,说明BaCl2溶液具有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚与苯甲醇互为同系物 | |
| B. | 利用碘酒解毒与酒精消毒均运用了蛋白质变性的性质 | |
| C. | 蔗糖与纤维素都是由C、H、O组成的高分子化合物 | |
| D. | 1mol油脂在酸性条件下充分水解,可制得3mol高级脂肪酸和1mol甘油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com