
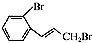 .
.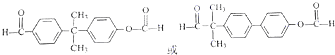 (只写一种).
(只写一种).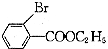 为原料制备二氢异苯并呋喃(结构简式如图
为原料制备二氢异苯并呋喃(结构简式如图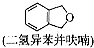 )的合成路线流程图(无机试剂可任选).
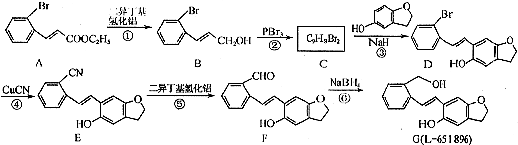
)的合成路线流程图(无机试剂可任选). 分析 (1)由D的结构简式,可知含有含氧官能团为羟基、醚键;
(2)对比B、C的分子式可知,B中-OH被-Br取代生成C;
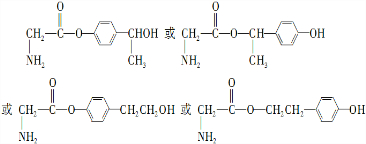
(3)G的一种同分异构体满足:Ⅰ.分子中含有2个苯环,Ⅱ.分子中含有7中不同化学环境的氢,Ⅲ.能水解生成两种有机物,说明含有酯基,一种产物能发生银镜反应,说明含有醛基,另一种产物既能发生银镜反应又能与FeCl3溶液发生显色反应,说明含有酚羟基,G的同分异构体含有醛基、羧酸与酚形成的酯基;
(4)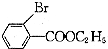 与CuCN反应得到
与CuCN反应得到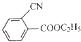 ,再与二异丁基氢化铝作用得到
,再与二异丁基氢化铝作用得到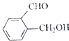 ,然后与NaBH4作用得到
,然后与NaBH4作用得到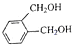 ,最后在浓硫酸作用下脱水生成
,最后在浓硫酸作用下脱水生成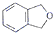 .
.
解答 解:(1)由D的结构简式,可知含有含氧官能团为羟基、醚键,故答案为:羟基、醚键;
(2)对比B、C的分子式可知,B中-OH被-Br取代生成C,属于取代反应,C的结构简式为: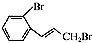 ,
,
故答案为:取代反应;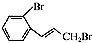 ;
;
(3)G的一种同分异构体满足:Ⅰ.分子中含有2个苯环,Ⅱ.分子中含有7中不同化学环境的氢,Ⅲ.能水解生成两种有机物,说明含有酯基,一种产物能发生银镜反应,说明含有醛基,另一种产物既能发生银镜反应又能与FeCl3溶液发生显色反应,说明含有酚羟基,G的同分异构体含有醛基、羧酸与酚形成的酯基,符合条件的同分异构体为: ,
,
故答案为: ;
;
(4)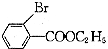 与CuCN反应得到
与CuCN反应得到 ,再与二异丁基氢化铝作用得到
,再与二异丁基氢化铝作用得到 ,然后与NaBH4作用得到
,然后与NaBH4作用得到 ,最后在浓硫酸作用下脱水生成
,最后在浓硫酸作用下脱水生成 ,合成路线流程图为:
,合成路线流程图为: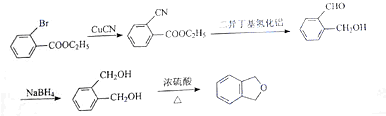 ,
,
故答案为: .
.
点评 本题考查有机物的合成,侧重考查学生信息获取与迁移运用能力、分析推理能力,(3)中同分异构体的书写为易错点、难点.


科目:高中化学 来源: 题型:解答题
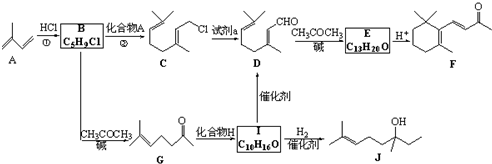
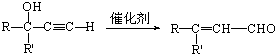 (R和R′表示烃基或氢)
(R和R′表示烃基或氢)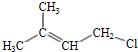 .
.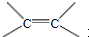 .
.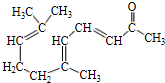 .
.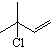 b.反应②的反应类型是加成反应
b.反应②的反应类型是加成反应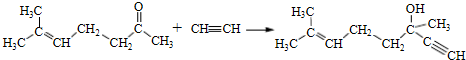 .
.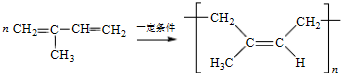 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
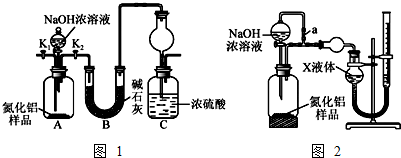
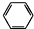
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
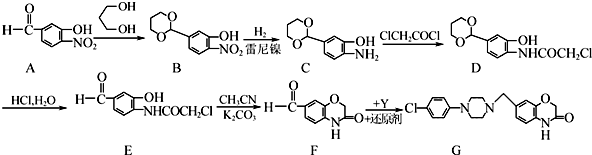
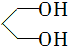 的名称为1,3丙二醇;设计步骤A→B的目的是保护醛基,防止被还原.
的名称为1,3丙二醇;设计步骤A→B的目的是保护醛基,防止被还原. .
. .
.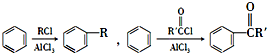
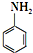 易氧化,酰胺基(
易氧化,酰胺基(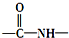 )难以被H2还原.
)难以被H2还原.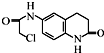 )是合成一种新型口服强心药的中间体,请写出以
)是合成一种新型口服强心药的中间体,请写出以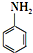 、ClCH2CH2COCl、ClCH2COCl为原料制备Z的合成路线流程图(无机试剂可任选).
、ClCH2CH2COCl、ClCH2COCl为原料制备Z的合成路线流程图(无机试剂可任选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
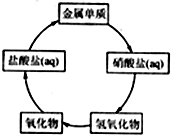 在一定条件下,五种含有同种金属元素的单质或其化合物,能按有图箭头方向实现一步转化(不含电解),该金属元素可能是 ( )
在一定条件下,五种含有同种金属元素的单质或其化合物,能按有图箭头方向实现一步转化(不含电解),该金属元素可能是 ( )| A. | ①② | B. | ②④ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3$\stackrel{盐酸}{→}$AlCl3溶液$\stackrel{蒸发}{→}$AlCl3 | |
| B. | Cu$\stackrel{稀硫酸}{→}$CuSO4溶液$\stackrel{冷却结晶}{→}$CuSO4•5H2O | |
| C. | Fe$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{NaOH}{→}$Fe(OH)3$\stackrel{△}{→}$Fe2O3 | |
| D. | Mg$\stackrel{空气中燃烧}{→}$MgO$\stackrel{HCl}{→}$MgCl2溶液$\stackrel{蒸发}{→}$MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
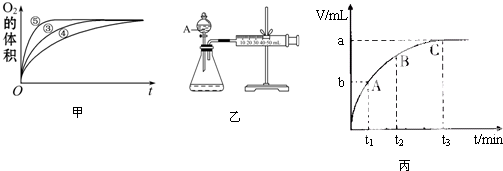
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片、银片,FeCl3溶液 | B. | 铜片、石墨棒,硝酸银溶液 | ||
| C. | 锌片、铜片,稀盐酸 | D. | 铜片、石墨棒,稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com