
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石雕像被酸雨腐蚀毁坏 | B. | 充有氢气的气球遇明火爆炸 | ||
| C. | 铁制菜刀生锈(Fe2O3•nH2O) | D. | 铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、蒸发、萃取 | B. | 分液、蒸馏、萃取 | C. | 萃取、蒸发、分液 | D. | 萃取、分液、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
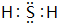 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 降温,使平衡左移,c(H+)减小,溶液呈碱性 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com