
下列物质间转化都能通过一步实现的是( )
A.Si→SiO2→H2SiO3→Na2SiO3
B.Al→Al2O3→NaAlO2→Al(OH)3
C.S→SO3→H2SO4→SO2
D.N2→NO2→HNO3→NO
科目:高中化学 来源: 题型:
用18 mol·L-1 浓硫酸配制100 mL 3.0 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④
⑤转移、洗涤 ⑥定容、摇匀 ⑦装瓶贴标签
完成下列问题:
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)第③步实验的操作是 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中_______________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水________________;
C.所用过的烧杯、玻璃棒未洗涤________________;
D.定容时俯视刻度线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是( )
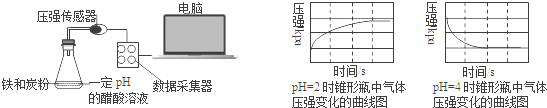
A. 溶液pH≤2时,生铁发生析氢腐蚀 B. 在酸性溶液中生铁可能发生吸氧腐蚀
C. 析氢腐蚀和吸氧腐蚀的速率一样快 D. 两溶液中负极反应均为:Fe﹣2e﹣=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应
2SO2(g)+O2(g) 2SO3(g) ∆H=-196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) ∆H=-196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
下列说法不正确的是( )x*k.
A.反应在前5min的平均速率为v (SO2)=0.08mol·L−1 ·min−1
B.保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v (正)> v (逆)
C.该温度,反应的平衡常数为11.25L·mol-1
D.相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
(1)软锰矿、闪锌矿与硫酸共热: MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O。
 (2)除去反应混合物中的不溶物
(2)除去反应混合物中的不溶物
(3)电解混合液MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
下列说法不正确的是 ( )
A.步骤⑴中每析出12.8g S沉淀共转移0.4mol电子
B.步骤⑴中ZnS的还原性大于MnSO4的还原性
C.电解时MnO2在阳极处产生
D.硫酸在生产中可循环使用
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是( )
A.原子半径:W>Z>Y>X>M
B.XZ2、X2M2、W2Z2均为直线型的共价化合物
C.由X元素形成的单质不一定是原子晶体
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,它的分
子构型是三角锥形。以下关于PH3的叙述正确的是
A.PH3分子中有未成键的孤对电子
B.P原子形成sp2杂化轨道
C.P-H键间的夹角为109°28′
D.PH3分子的P-H键是非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com