
①称取试样
②称取试样
请完成下列问题:?
(1)步骤①称取的试样中,所有卤原子的物质的量之和是_____________mol,该试样中碘原子的物质的量是______________mol。?
(2)列式计算原混合物中溴的质量分数和氯的质量分数。
?
解析:(2)![]() (Cl)+
(Cl)+![]() (Br)=0.020 mol-0.004 mol=0.016 mol?
(Br)=0.020 mol-0.004 mol=0.016 mol?
![]() (AgCl)+
(AgCl)+ ![]() (AgBr)=
(AgBr)=
![]() (Br)=(
(Br)=(
![]() (Br)=0.007 51 mol×
(Br)=0.007 51 mol×
![]() (Cl)=0.016 0 mol-0.007 51 mol=0.008 49 mol?
(Cl)=0.016 0 mol-0.007 51 mol=0.008 49 mol?
![]() (Cl)=0.008 49 mol×
(Cl)=0.008 49 mol×
答案:(1)0.0200 0.004(此处对有效数字不作要求)
(2)12.0% 6.03%??


科目:高中化学 来源: 题型:
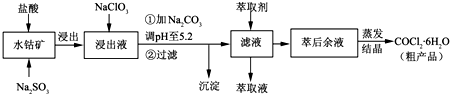
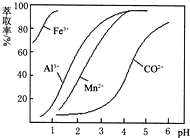
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:志鸿系列全优设计必修一化学鲁科版 鲁科版 题型:038
有一种可溶性氯化物、溴化物、碘化物的混合物,对其进行如下测定:
①称取试样5.00 g,溶于水后加入足量AgNO3溶液,使卤离子完全沉淀为卤化银,质量为3.57 g.将该卤化银加热并通入氯气使AgBr、AgI完全转化为AgCl后,其质量变为2.87 g.
②称取试样15.00 g,溶于水后加入氯化亚钯(PdCl2)处理后,其中只有碘化物转化为PdI2沉淀,该沉淀的质量为2.16 g.
请完成下列问题:
(1)步骤①称取的试样中,所有卤原子的物质的量之和是________mol,该试样中碘原子的物质的量是________mol.
(2)列式计算原混合物中溴的质量分数和氯的质量分数.
查看答案和解析>>
科目:高中化学 来源: 题型:
①称取试样
②称取试样
请完成下列问题:?
(1)步骤①称取的试样中,所有卤原子的物质的量之和是_____________mol,该试样中碘原子的物质的量是______________mol。?
(2)列式计算原混合物中溴的质量分数和氯的质量分数。
?
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种可溶性氯化物、溴化物、碘化物的混合物,对其进行如下测定:
①称取试样5.00 g,溶于水后加入足量AgNO3溶液,使卤离子完全沉淀为卤化银,质量为3.57 g。将该卤化银加热并通入氯气使AgBr、AgI完全转化为AgCl后,其质量变为2.87 g。
②称取试样15.00 g,溶于水后加入氯化亚钯(PdCl2)处理后,其中只有碘化物转化为PdI2沉淀,该沉淀的质量为2.16 g。
请完成下列问题:
(1)步骤①称取的试样中,所有卤原子的物质的量之和是_____________mol,该试样中碘原子的物质的量是______________mol。
(2)列式计算原混合物中溴的质量分数和氯的质量分数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com