
 ��֪X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�ܼ���������p�ܼ���������������Zԭ��L������2�ԳɶԵ��ӣ�Q�ǵ��������е縺������Ԫ�أ�E�ĵ����dz�����Ψһ��Һ̬�ķǽ�������ش��������⣺
��֪X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�ܼ���������p�ܼ���������������Zԭ��L������2�ԳɶԵ��ӣ�Q�ǵ��������е縺������Ԫ�أ�E�ĵ����dz�����Ψһ��Һ̬�ķǽ�������ش��������⣺���� X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬����Xԭ�Ӻ��������Ϊ6����XΪ̼Ԫ�أ�Zԭ��L������2�ԳɶԵ��ӣ���Zԭ�Ӻ�������Ų�Ϊ1s22s22p4����ZΪ��Ԫ�أ�Yԭ����������̼Ԫ������Ԫ��֮�䣬��YΪ��Ԫ�أ�Q�ǵ��������е縺������Ԫ�أ�QΪClԪ�أ�E�ĵ����dz�����Ψһ��Һ̬�ķǽ�����EΪBrԪ�أ�
��1��ͬ����������ҵ�һ�����ܳ��������ƣ�����ԭ��2p�ܼ���3�����ӣ����ڰ����ȶ�״̬�������ϵͣ�ʧȥ������Ҫ�����ϸߣ�
Y�ļ��⻯��ΪNH3��ȷ��Nԭ�Ӽ۲���Ӷ���������ȷ��Nԭ���ӻ���ʽ�����ݿռ�ṹ�ж�������������Ƿ��غϣ�ȷ�����Ӽ������⣻
��2��EΪBrԪ�أ�ԭ�Ӻ��������Ϊ35�����ݺ�������Ų�������д��
��3��CO2������Cԭ�ӳ�2��C=O˫����˫���к���1���Ҽ���1���м���
��4����Ԫ�صĵ縺�Ժ�ǿ��ˮ����֮���������������۷е����ߣ�
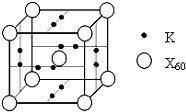
��5�����ݾ�̯�����㾧����X60���ԭ�Ӹ������ݴ˽��
��� �⣺X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬����Xԭ�Ӻ��������Ϊ6����XΪ̼Ԫ�أ�Zԭ��L������2�ԳɶԵ��ӣ���Zԭ�Ӻ�������Ų�Ϊ1s22s22p4����ZΪ��Ԫ�أ�Yԭ����������̼Ԫ������Ԫ��֮�䣬��YΪ��Ԫ�أ�Q�ǵ��������е縺������Ԫ�أ�QΪClԪ�أ�E�ĵ����dz�����Ψһ��Һ̬�ķǽ�����EΪBrԪ�أ�
��1��ͬ����������ҵ�һ�����ܳ��������ƣ�����ԭ��2p�ܼ���3�����ӣ����ڰ����ȶ�״̬�������ϵͣ�ʧȥ������Ҫ�����ϸߣ���NԪ�صĵ�һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������C��O��N��
Y�ļ��⻯��ΪNH3��Ϊ�����νṹ��Nԭ�Ӽ۲���Ӷ���Ϊ3+$\frac{5-1��3}{2}$=4��Nԭ���ӻ���ʽΪsp3������������������IJ��غϣ����ڼ��Է��ӣ�
�ʴ�Ϊ��C��O��N�������Σ�sp3��N���ԣ�
��2��EΪBrԪ�أ�ԭ�Ӻ��������Ϊ35����������Ų�ʽΪ��1s22s22p63s23p63d104s24p5���ʴ�Ϊ��1s22s22p63s23p63d104s24p5��
��3��CO2������Cԭ�ӳ�2��C=O˫����˫���к���1���Ҽ���1���м�����CO2�����к���2���м����ʴ�Ϊ��2��
��4����Ԫ�صĵ縺�Ժ�ǿ��ˮ����֮���������������۷е����ߣ���Z�⻯��ķе��Q�⻯��ķе�ߣ�
�ʴ�Ϊ����Ԫ�صĵ縺�Ժ�ǿ��ˮ����֮���������������۷е����ߣ�
��5���ɾ����ṹ��֪��������X60��ĿΪ1+8��$\frac{1}{8}$=2��Kԭ����ĿΪ2��6��$\frac{1}{2}$=6���ʾ�����X60���ԭ�Ӹ���֮��Ϊ2��6=1��3���ʴ�Ϊ��1��3
���� �����Ƕ����ʽṹ�Ŀ��飬�漰��������Ų����ɡ������ܡ���ѧ�����������������ȣ��Ѷ��еȣ�ע�����þ�̯�����о����ļ��㣮


 �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��Һ�����CO32-+2 H+=H2O+CO2�� | |
| B�� | ��������Һ��ͭ��Cu+Ag+=Cu2++Ag | |
| C�� | ��������ˮ��Ӧ��K+H2O�TK++OH-+H2�� | |
| D�� | �ô����ˮ����2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | S��s��+O2��g����SO2��g��+Q1kJ��S��g��+O2��g����SO2��g��+Q2kJ | |
| B�� | H2��g��+$\frac{1}{2}$O2��g����H2O��l��+Q1kJ��H2��g��+$\frac{1}{2}$O2��g����H2O��g��+Q2kJ | |
| C�� | NaOH��aq��+HCl��aq����NaCl��aq��+H2O��l��+Q1kJ NaOH��aq��+HAc��aq����NaAc��aq��+H2O��l��+Q2kJ | |
| D�� | H2��g��+Cl2��g����2HCl��g��+Q1kJ��H2��g��+I2��g����2HI��g��+Q2kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ��Ӧʱ��t/s | 1 | 4 | 9 | 16 |
| �Ʋ���y/nm | a | 2a | 3a | 4a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
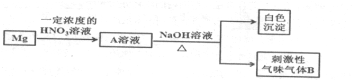
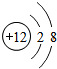 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
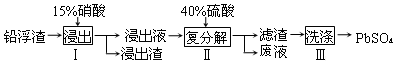
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| W | X | |
| Y | Z |
| A�� | Y����̬�⻯�����ȶ� | B�� | Z�ĵ��������ӻ�ԭ����ǿ | ||
| C�� | X���ʳ����»�ѧ���ʻ��� | D�� | Y��ԭ��������W��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѧʽ | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp��Ka | Ksp=1.8��10-10 | Ksp=9.0��10-12 | Ka=1.8��10-5 | Ka=3.0��10-8 | Ka1=4.1��10-7 Ka2=5.6��10-11 |
| A�� | ��ͬŨ��CH3COONa��NaClO�Ļ����Һ�У���������Ũ�ȵĴ�С��ϵ�ǣ�c��Na+����c��ClO-����c��CH3COO-����c��OH-����c��H+�� | |
| B�� | ����������Һ��ͨ������CO2�����ӷ���ʽΪ��2ClO-+CO2+H2O=CO32-+2HClO | |
| C�� | ��0.1 mol•L-1CH3COOH��Һ�еμ�NaOH��Һ����c��CH3COOH����c��CH3COO-��=5��9����ʱ��Һ��pH=5 | |
| D�� | ��Ũ�Ⱦ�Ϊ1.0��10-3 mol•L-1��KCl��K2CrO4�����Һ�еμ�1.0��10-3 mol•L-1��AgNO3��Һ��CrO42-���γɳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ۺ��������ԣ�X��Y | B�� | X��Y��Z���γ����ӻ����� | ||
| C�� | W���γ�˫ԭ�ӷ��� | D�� | M��W�γɵĻ����ﺬ���Թ��ۼ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com